International Journal of Molecular Sciences, 20/08/2025
Mở đầu
Mặc dù y học hiện đại đã đạt được nhiều tiến bộ đáng kể, song bệnh đái tháo đường, đặc biệt là đái tháo đường loại 1 (T1D), vẫn là một thách thức sức khỏe nghiêm trọng. Những người mắc T1D có nguy cơ cao gặp nhiều biến chứng, trong đó các rối loạn về mạch máu là một trong những biến chứng nghiêm trọng và đe dọa tính mạng nhất. Theo thời gian, những bất thường này dẫn đến các hậu quả lâm sàng nghiêm trọng như bệnh thận do đái tháo đường, bệnh võng mạc, bệnh lý thần kinh ngoại biên và các bệnh tim mạch, bao gồm bệnh mạch vành.
Yếu tố trung tâm trong sự phát triển của các biến chứng này là rối loạn chức năng nội mô – một đặc trưng nổi bật của bệnh đái tháo đường. Lớp nội mô, bao gồm một lớp tế bào mỏng lót bên trong mạch máu, đóng vai trò quan trọng trong việc duy trì cân bằng nội môi mạch máu thông qua điều hòa lưu lượng máu, phản ứng viêm và quá trình đông máu. Ở bệnh nhân tiểu đường, tình trạng tăng đường huyết mạn tính và stress oxy hóa làm suy giảm chức năng nội mô, dẫn đến tổn thương mạch máu. Nồng độ glucose cao kích thích sự sản sinh quá mức các loại oxy phản ứng (ROS) như hydrogen peroxide (H2O2) trong tế bào nội mô.
ROS là những phân tử có tính oxy hóa cao, gây tổn thương cho các thành phần tế bào như lipid, protein và DNA. Stress oxy hóa làm tổn hại lớp nội mô, làm giảm khả năng sản xuất nitric oxide (NO) – một phân tử quan trọng giúp giãn mạch và duy trì sức khỏe mạch máu. Hệ quả là mạch máu trở nên dễ bị viêm, huyết khối và xơ vữa, góp phần thúc đẩy tiến triển của các biến chứng đái tháo đường.
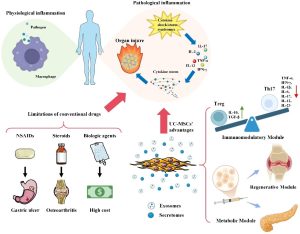
Trong những năm gần đây, sinh học tế bào gốc đã nổi lên như một lĩnh vực đột phá trong điều trị bệnh và y học tái tạo. Tế bào gốc, với khả năng tự làm mới và biệt hóa thành nhiều loại tế bào khác nhau, mang lại tiềm năng to lớn trong điều trị nhiều bệnh lý, bao gồm bệnh tim mạch, rối loạn miễn dịch, ung thư, đái tháo đường và tổn thương các cơ quan như gan, tim, và não. Trong số các loại tế bào gốc, tế bào gốc trung mô (MSCs) nhận được sự quan tâm đặc biệt nhờ tính linh hoạt và khả năng điều trị đa dạng. MSCs là các tế bào đa tiềm năng có thể được tách chiết từ nhiều loại mô trưởng thành như mô mỡ, tủy xương, dây rốn, tủy răng và nhau thai. Nhờ khả năng di chuyển đến vùng tổn thương và điều hòa đáp ứng miễn dịch, MSCs trở thành ứng viên đầy hứa hẹn trong điều trị các bệnh lý chuyển hóa và miễn dịch.
MSCs được tách chiết từ các vùng khác nhau của nhau thai sản phụ mang thai đủ tháng, bao gồm tế bào gốc trung mô từ màng rụng nền (decidua basalis MSCs, DBMSCs), màng rụng thành (decidua parietalis MSCs, DPMSCs) và nhung mao nhau (chorionic villus MSCs, CVMSCs), được gọi chung là tế bào gốc trung mô có nguồn gốc từ nhau thai (placenta-derived MSCs, pMSCs). Những tế bào này thể hiện khả năng biệt hóa theo hướng trung mô và tiết ra nhiều cytokine, yếu tố tăng trưởng và phân tử điều hòa miễn dịch. Các nghiên cứu cho thấy pMSCs có tác dụng bảo vệ tế bào nội mô khỏi sự hoạt hóa viêm và stress oxy hóa, đặc biệt là tổn thương do H2O2 gây ra.
Những phát hiện này nhấn mạnh tiềm năng điều trị của pMSCs trong việc làm giảm rối loạn chức năng nội mô, khiến chúng trở thành ứng viên đáng quan tâm cho các nghiên cứu sâu hơn trên mô hình động vật về biến chứng mạch máu do đái tháo đường.
Phương pháp
Phân lập và nuôi cấy pMSCs
Nhau thai đủ tháng (38-40 tuần) được thu từ người hiến khỏe mạnh có ký cam kết đồng thuận. Tế bào gốc trung mô nhau thai (pMSCs) được tách từ vùng màng rụng nền, nuôi trong môi trường DMEM-F12 bổ sung 10% huyết thanh nhau thai bò và kháng sinh, duy trì ở 37°C, 5% CO2. Chỉ các mẫu có tỷ lệ tế bào sống trên 90% được sử dụng, và tế bào từ 20 nhau thai được gộp để giảm sai lệch giữa các mẫu.
Tạo mô hình chuột đái tháo đường
24 chuột đực C57BL/6 (8 tuần tuổi) được chia thành 2 nhóm: nhóm đối chứng và nhóm mô hình bệnh lý. Đái tháo đường loại 1 được gây ra bằng cách tiêm phúc mạc streptozotocin (STZ, 40 mg/kg/ngày) trong 5 ngày liên tiếp. Chuột có glucose máu cao hơn 150 mg/dL trong hai lần đo liên tiếp được xem là mắc đái tháo đường. Ngày 51 sau tiêm STZ, các mô thận, tim và võng mạc được thu để phân tích mô học.
Thử nghiệm tiêm pMSCs
Chuột được chia thành bốn nhóm, mỗi nhóm gồm 6 cá thể: đối chứng, chỉ tiêm pMSC, đái tháo đường, và đái tháo đường + tiêm pMSC. Nhóm đái tháo đường + tiêm pMSC được tiêm phúc mạc 1 × 106 (1 triệu) tế bào pMSCs hòa trong 0,2 mL PBS, trong khi nhóm đối chứng chỉ tiêm PBS.
Đánh giá dung nạp glucose
Sau khi nhịn ăn 14 giờ, chuột được tiêm phúc mạc glucose liều 2 mg/g trọng lượng cơ thể. Glucose máu được đo tại các mốc 0, 15, 30, 45, 60, 90 và 120 phút.
Đánh giá dung nạp insulin
Sau khi nhịn ăn 2 giờ, chuột được tiêm insulin (0,75 U/kg, trong phúc mạc), và glucose máu được theo dõi trong 120 phút.
Nhuộm và phân tích mô học
Các mô thận, tim và võng mạc được cố định trong dung dịch paraformaldehyde 4%, đúc paraffin và cắt lát dày 4 µm. Phiến mô được nhuộm Hematoxylin & Eosin và Picrosirius Red, sau đó đo diện tích cầu thận, độ dày các lớp võng mạc và tỷ lệ collagen (CPA).
Kết quả
Điều trị bằng pMSCs không giúp cải thiện khả năng điều hòa glucose hay độ nhạy insulin, cho thấy pMSCs không ảnh hưởng trực tiếp đến chuyển hóa glucose toàn thân.
Phân tích mô học cho thấy điều trị bằng pMSCs làm giảm đáng kể sự lắng đọng collagen trong mô thận của chuột đái tháo đường so với nhóm không điều trị. Kết quả này cho thấy pMSCs có khả năng làm giảm xơ hóa thận và bảo tồn cấu trúc mô thận, thể hiện vai trò bảo vệ đối với bệnh thận đái tháo đường.
Bên cạnh đó, điều trị bằng pMSCs giúp phục hồi đáng kể độ dày võng mạc tổng thể và các lớp cấu trúc (lớp đám rối ngoài, lớp nhân ngoài và lớp tế bào cảm thụ ánh sáng) so với nhóm không điều trị. Kết quả này cho thấy pMSC có tác dụng bảo vệ cấu trúc võng mạc và có thể ngăn ngừa tiến triển của bệnh võng mạc đái tháo đường.
Cuối cùng, kết quả mô học tim cho thấy điều trị bằng pMSCs làm giảm đáng kể sự tích tụ collagen trong mạch máu của chuột đái tháo đường. Điều này chứng tỏ pMSCs có tác dụng bảo vệ tim, hạn chế xơ hóa mạch máu, duy trì tính toàn vẹn cấu trúc mạch và giảm nguy cơ biến chứng tim mạch liên quan đến đái tháo đường.
Kết luận
Nghiên cứu này cho thấy việc sử dụng tế bào gốc trung mô có nguồn gốc từ nhau thai theo đường toàn thân không cải thiện độ nhạy insulin ở chuột đái tháo đường cảm ứng bằng STZ. Tuy nhiên, pMSC có hiệu quả trong việc ngăn chặn tiến triển của các biến chứng vi mạch do đái tháo đường, bao gồm bệnh thận, bệnh võng mạc và tổn thương mạch máu tim. Những phát hiện này nhấn mạnh tiềm năng điều trị đầy hứa hẹn của pMSC trong việc phòng ngừa và đảo ngược các biến chứng mạch máu do đái tháo đường. Cần có thêm các nghiên cứu để làm rõ cơ chế bảo vệ này trước khi pMSCs có thể được ứng dụng trong lâm sàng.
Tài liệu tham khảo
Bài viết được dịch và tóm tắt từ bài báo (nếu có): Basmaeil, Y., Bakillah, A., Al Subayyil, A. M., Bin Kulayb, H. N., AlRodayyan, M. A., Al Otaibi, A., Mubarak, S. A. S., Alamri, H. S., Kondkar, A. A., Iqbal, J., & Khatlani, T. (2025). Placenta-Derived Mesenchymal Stem Cells (pMSCs) Reverse Diabetes-Associated Endothelial Complications in a Preclinical Animal Model. International Journal of Molecular Sciences, 26(16), 8057.
https://doi.org/10.3390/ijms26168057
Nguồn: International Journal of Molecular Sciences