Tạp chí Quốc tế về Khoa học Phân tử, 29/11/2022
Emérito Carlos Rodríguez-Merchán1,2
- Khoa Phẫu thuật Chỉnh hình, Bệnh viện Đại học La Paz, Paseo de la Castellana 261, 28046 Madrid, Tây Ban Nha; ecrmerchan@hotmail.com
- Nghiên cứu Phẫu thuật Xương khớp, Bệnh viện Viện Nghiên cứu Sức khỏe La Paz—IdiPAZ (Bệnh viện Đại học La Paz—Đại học Tự trị Madrid), 28046 Madrid, Tây Ban Nha
Tóm tắt: Hơn 10% dân số thế giới bị viêm xương khớp (OA) đầu gối, với nguy cơ mắc bệnh suốt đời là 45%. Các phương pháp điều trị đau viêm khớp gối hiện nay như sau: kiểm soát cân nặng; điều trị bằng thuốc uống (thuốc chống viêm không steroid, paracetamol, opioids); dụng cụ hỗ trợ cơ học (nạng, khung tập đi, nẹp, nẹp chỉnh hình); tập thể dục trị liệu; và tiêm nội khớp corticosteroid, axit hyaluronic và huyết tương giàu tiểu cầu (PRP). Vấn đề là các phương pháp điều trị như vậy thường chỉ làm giảm đau khớp trong một thời gian ngắn. Đối với tiêm nội khớp, corticosteroid giảm đau trong vài tuần, trong khi axit hyaluronic và PRP giảm đau trong vài tháng. Khi các phương pháp điều trị trên không kiểm soát được cơn đau đầu gối, phẫu thuật thay khớp gối toàn phần (TKA) thường được chỉ định; tuy nhiên, mặc dù kỹ thuật phẫu thuật rất hiệu quả, nhưng nó có thể liên quan đến các biến chứng y tế sau phẫu thuật (liên quan đến phẫu thuật). Do đó, điều cần thiết là tìm kiếm các phương pháp điều trị thay thế an toàn và hiệu quả cho TKA. Gần đây, đã có nhiều nghiên cứu về việc tiêm tế bào gốc trung mô (MSC) vào trong khớp để điều trị thoái hóa khớp gối. Bài viết này xem xét các thông tin mới nhất về cơ chế hoạt động phân tử của MSC và lợi ích điều trị tiềm năng của chúng trong thực hành lâm sàng ở bệnh nhân bị viêm khớp gối gây đau. Mặc dù hầu hết các ấn phẩm gần đây đều tuyên bố rằng tiêm MSC nội khớp làm giảm đau khớp trong thời gian ngắn, nhưng hiệu quả của chúng vẫn còn gây tranh cãi do thông tin khoa học hiện có về MSC là thiếu quyết đoán. Trước khi khuyến cáo tiêm MSC nội khớp thường xuyên ở những bệnh nhân bị viêm khớp gối gây đau, cần có thêm các nghiên cứu so sánh MSC với giả dược. Hơn nữa, cần có một quy trình chuẩn để tiêm MSC nội khớp trong viêm khớp gối.
- Giới thiệu
Viêm xương khớp nguyên phát (OA) là một bệnh thoái hóa gây đau khớp nghiêm trọng, không dễ kiểm soát ở những bệnh nhân mắc phải. Tuổi thọ trung bình của dân số thế giới ngày càng tăng và tỷ lệ béo phì ngày càng tăng khiến viêm khớp gối trở thành gánh nặng kinh tế ngày càng tăng đối với các hệ thống chăm sóc sức khỏe trên toàn thế giới [1,2]. Hơn 10% dân số thế giới bị thoái hóa khớp gối, với nguy cơ suốt đời bị thoái hóa khớp gối là 45% [3].
Hiện nay, các phương pháp điều trị đau liên quan đến viêm khớp bao gồm kiểm soát cân nặng; điều trị bằng thuốc uống (thuốc chống viêm không steroid, paracetamol, opioids); dụng cụ hỗ trợ cơ học (nạng, khung tập đi, nẹp, nẹp chỉnh hình); tập thể dục trị liệu; và tiêm nội khớp corticosteroid, axit hyaluronic và huyết tương giàu tiểu cầu (PRP) [4,5]. Tuy nhiên, những phương pháp điều trị này có xu hướng giảm đau khớp chỉ trong thời gian ngắn – vài tuần đối với corticosteroid và vài tháng đối với axit hyaluronic và PRP [6,7].
Cho rằng viêm khớp gối là một bệnh mãn tính, điều trị lâu dài thường đòi hỏi phẫu thuật thay khớp gối toàn phần (TKA). Mặc dù đây là một kỹ thuật phẫu thuật hiệu quả nhưng không tránh khỏi các biến chứng. Do đó, những bệnh nhân bị viêm khớp gối không thể kiểm soát cơn đau bằng các biện pháp bảo tồn và không tích cực đã đề cập trước đó đã tiếp tục tìm kiếm các liệu pháp không tích cực như TKA, chẳng hạn như tiêm tế bào gốc trung mô (MSC) vào khớp [1,8 ,9].
MSC là các tế bào cư trú trong tủy xương khác với tế bào gốc tạo máu, có khả năng tăng sinh rộng và khả năng biệt hóa thành các loại tế bào khác nhau, bao gồm tế bào mỡ, tế bào cơ tim, tế bào sụn, tế bào cơ, tế bào thần kinh và tế bào xương. MSC rất cần thiết để duy trì cân bằng nội môi trong tủy xương và kiểm soát sự trưởng thành của cả tế bào tạo máu và tế bào không tạo máu. Mặc dù các tế bào được đặc trưng bởi sự biểu hiện của nhiều kháng nguyên bề mặt, nhưng dường như không có kháng nguyên nào được biểu hiện duy nhất trên MSC. Ngoài tủy xương, MSC cũng nằm trong các mô khác, chẳng hạn như mô mỡ, máu cuống rốn, gan và mô bào thai, và máu ngoại vi [10].
Theo Jang và cộng sự, tế bào gốc phôi và tế bào gốc đa năng cảm ứng (induced pluripotent stem cells) được biến đổi thành tế bào sụn hoặc MSC; do đó, chúng có thể được tiêm bằng cách tiêm vào khoang khớp ở bệnh nhân viêm khớp gối. MSC cũng được biết là có đặc tính điều hòa miễn dịch, ví dụ, khả năng tăng cường phục hồi sụn và phục hồi sức khỏe đầu gối [11].
Mục đích của bài viết này là xem xét các cơ chế hoạt động phân tử của MSC và hiệu quả của việc tiêm nội khớp của chúng ở những bệnh nhân bị viêm khớp gối gây đau.
- Cơ chế hoạt động phân tử của MSC
Kết quả tìm kiếm PubMed (MEDLINE) về các nghiên cứu liên quan đến MSC trong viêm khớp gối đã được phân tích. Các tìm kiếm được thực hiện từ khi bắt đầu công cụ tìm kiếm cho đến ngày 31 tháng 10 năm 2022 bằng cách sử dụng từ khóa “MSC thoái hóa khớp gối”. Chỉ những nghiên cứu về MSC trong viêm khớp gối mà tác giả cho là đáng quan tâm nhất mới được đưa vào. PubMed tìm thấy 391 bài báo, trong đó có 77 bài được chọn. Những bài dường như liên quan trực tiếp nhất đến tiêu đề của bài báo này đã được chọn, tức là 77 bài báo.
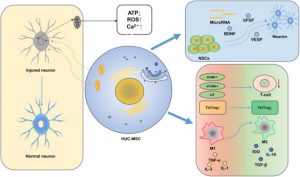
MSC đóng vai trò quan trọng trong quá trình sửa chữa và tái tạo (Hình 1). Chúng bao gồm giảm tế bào chết để liên tục thay thế các tế bào mất đi, tiết ra các yếu tố dinh dưỡng giúp ổn định chất nền ngoại bào và ức chế kích hoạt tế bào miễn dịch để ngăn ngừa viêm nhiễm [12].
Trong một nghiên cứu, exosome được thu hoạch từ ESC-MSC trong môi trường nuôi cấy có điều kiện bằng quy trình ly tâm tuần tự. Sau đó, ESC-MSC hoặc exosome của chúng được tiêm vào bên trong. Một mô hình in vitro với các tế bào sụn sơ cấp của chuột được kích thích bằng interleukin-1 beta (IL-1β) đã được sử dụng để đánh giá tác động của môi trường điều hòa có hoặc không có exosome và liều chuẩn độ của exosome bị cô lập trong hai ngày, trước khi phân tích hóa mô miễn dịch hoặc Western blot. Sự mất ổn định của phẫu thuật sụn chêm (DMM) trên đầu gối của chuột C57BL/6 J đã được sử dụng làm mô hình viêm khớp [13]. Kết quả cho thấy rằng exosome từ MSCs do tế bào gốc phôi người (ESC-MSCs) gây ra có tác động điều trị có lợi đối với viêm khớp bằng cách cân bằng giữa sản xuất và phân hủy chất nền ngoại bào (ECM) của tế bào sụn [13].
Sử dụng chuột Sprague–Dawley được thiết kế có các tế bào sụn viêm khớp do collagenase II và IL-1β gây ra, axit ribonucleic malat-1 dài không mã hóa từ các túi ngoại bào (EVs) thu nhận từ hMSC đã thúc đẩy sự tăng sinh tế bào sụn, giảm viêm sụn và sụn thoái hóa và tăng cường sửa chữa tế bào sụn [14].
Một nghiên cứu của Yang và cộng sự đã sử dụng tropoelastin làm môi trường tiêm và so sánh nó với môi trường cổ điển, chẳng hạn như nước muối sinh lý, axit hyaluronic và huyết tương giàu tiểu cầu (PRP), trong tiêm MSC nội khớp. Các tác giả phát hiện ra rằng tropoelastin đã thúc đẩy sự di cư của các MSC đệm mỡ dưới xương bánh chè (IPFP-MSC) và bảo vệ sụn đầu gối khỏi tổn thương viêm khớp bằng cách tăng cường sự kết dính của tế bào và kích hoạt con đường protein kinase 1/2/vinculin điều hòa tín hiệu ngoại bào. Những phát hiện này đã cung cấp những hiểu biết mới về việc tiêm MSC nội khớp để điều trị viêm khớp [15].
Trong một nghiên cứu, các MSC nuôi cấy có nguồn gốc từ ba loại mô (tủy xương, mô mỡ và màng hoạt dịch) được xử lý bằng IL-1β và yếu tố hoại tử khối u-alpha hoặc không đạt được môi trường điều hòa. Mỗi môi trường điều hòa được sử dụng để phân tích các yếu tố cận tiết liên quan đến phục hồi sụn bằng phương pháp sắc ký lỏng khối phổ song song. MSC từ các mô này biểu hiện 93 protein trong trường hợp bình thường và 105 protein trong trường hợp viêm nhiễm [16]. Các protein được biểu hiện khác nhau có thể góp phần tái tạo sụn bị hư hỏng.
Trong mô hình nuôi cấy màng hoạt dịch đã được nhũ tương, MSC được giải phóng từ màng hoạt dịch đi qua môi trường vào đĩa nuôi cấy không tiếp xúc [17]. Các tác giả phát hiện ra rằng, ở đầu gối bị viêm khớp, các MSC nội sinh có thể được huy động một cách tương tự từ màng hoạt dịch qua hoạt dịch, tác động vào phương cách bảo vệ. Tuy nhiên, trong quá trình tự nhiên của OA, số lượng MSC được huy động là có hạn, dẫn đến sự tiến triển của OA. Trong một mô hình viêm khớp ở chuột, người ta cũng nhận thấy rằng việc tiêm MSC hoạt dịch đã ức chế sự tiến triển của thoái hóa sụn. Các MSC hoạt dịch được tiêm di chuyển vào màng hoạt dịch, duy trì các đặc tính MSC của chúng và tăng biểu hiện gen của TSG-6, PRG-4 và protein hình thái xương-2. Nghĩa là, các MSC hoạt dịch ngoại sinh có thể tạo điều kiện thuận lợi cho quá trình chống viêm, bôi trơn và hình thành chất nền sụn ở đầu gối bị thoái hóa khớp [17].
Người ta đã chứng minh rằng tình trạng sưng mãn tính dẫn đến việc chuyển Ca2+ dư thừa từ mạng lưới nội chất sang ty thể, dẫn đến tình trạng quá tải canxi của ty thể và gây hại thêm cho ty thể [18]. Hơn nữa, trong điều kiện viêm mãn tính, ty thể bị tổn thương tích tụ theo thời gian trong MSC do giảm phân bằng cách kích hoạt con đường Wnt/-catenin, làm suy yếu sự biệt hóa của MSC. Zhai et al. đã phân lập các MSC đặc trưng của mô trong dây chằng nha chu, được gọi là tế bào gốc dây chằng nha chu, từ những bệnh nhân khỏe mạnh và bệnh nhân bị viêm nha chu. Dựa trên phát minh cơ học, các hạt nano phản ứng với môi trường vi mô nội bào (esteraza và độ pH thấp) được tạo ra để thu giữ Ca2+ xung quanh ty thể trong MSC để kiểm soát dòng canxi trong ty thể chống lại rối loạn chức năng của ty thể. Các hạt nano có thể giải phóng siRNA khỏi MSC để hạn chế con đường Wnt/β-catenin và kiểm soát quá trình giảm phân của ty thể bị rối loạn chức năng ban đầu. Các hạt nano nói trên (“máy sửa chữa nano”) đã tái lập về mặt sinh lý hoạt động của ty thể và MSC, đây có thể là một liệu pháp hiệu quả mới chống lại viêm khớp [18]. Hình 2 tóm tắt hiệu ứng di động sự hoạt động của MSC.

- Hiệu quả của tiêm MSC nội khớp trong bệnh thoái hóa khớp gối
- Các nghiên cứu thực nghiệm
Một đánh giá có hệ thống về các nghiên cứu trên động vật đã kết luận rằng việc tiêm MSC vào trong khớp không thể được khuyến nghị cho các thử nghiệm lâm sàng viêm khớp gối. Họ cũng tuyên bố rằng, dựa trên giá trị bên trong và bên ngoài của các nghiên cứu trên động vật, cần phải có các nghiên cứu thực nghiệm chất lượng cao và nỗ lực hơn nữa để chuyển các nghiên cứu tiền lâm sàng sang thử nghiệm lâm sàng vào thời điểm đó (năm 2018) [19].
Tính an toàn và hiệu quả của việc tiêm MSC đồng loài vào trong khớp đã được nghiên cứu trong một thí nghiệm viêm khớp ở lợn sau khi cắt bỏ sụn chêm ở đầu gối cả hai bên [20]. Các MSC có nguồn gốc từ tủy xương (BM-MSC) được dán nhãn bằng các hạt nano oxit sắt siêu thuận từ (SPIO) để cho phép theo dõi tế bào bằng hình ảnh cộng hưởng từ (MRI). Ở nồng độ ≤ 20 µg/mL, hạt nano SPIO không độc đối với BM-MSC. Bốn tuần sau phẫu thuật, các tổn thương viêm khớp đã được ghi nhận trên MRI. Trong khoảng thời gian từ 8 đến 24 giờ sau khi tiêm, các BM-MSC được đánh dấu SPIO đã được dịch chuyển vào phần sụn bị hư hỏng. Ngoài ra, phân tích mô học và hóa mô miễn dịch không tìm thấy sự khác biệt đáng kể giữa đầu gối phải (nhóm điều trị) và đầu gối trái (nhóm đối chứng). Nồng độ thích hợp của các hạt nano SPIO để dán nhãn BM-MSC là 20 µg/mL, trong khi các MSC đồng loài có thể di chuyển vào phần sụn bị suy yếu và tích tụ xung quanh nó. Không có sự khác biệt đáng kể nào được tìm thấy giữa nhóm điều trị và nhóm đối chứng [20].
Một nghiên cứu đã so sánh hiệu quả của: liệu pháp sóng xung kích ngoài cơ thể (ESWT), MSC từ Wharton Jelly (WJ-MSC) và sự kết hợp của ESWT và WJ-MSC trong viêm khớp gối sớm ở chuột. Qua kết quả nghiên cứu bệnh học, chụp cắt lớp vi tính và nhuộm hóa mô miễn dịch đã chứng minh rằng cả ba lựa chọn đều cải thiện đáng kể tình trạng thoái hóa khớp gối giai đoạn sớm. Nhóm điều trị kết hợp đã làm tăng thể tích xương và độ dày bè xương, cũng như giảm viêm màng hoạt dịch hơn so với ESWT hoặc WJ-MSC đơn thuần. Tuy nhiên, không có sự khác biệt đáng kể trong ESWT và WJ-MSC kết hợp, như được thể hiện trong các biểu thức của IGF-1 và yếu tố tăng trưởng chuyển dạng (TGF)-β1, và sự giảm hoạt động TUNEL ở đầu gối viêm khớp. Hơn nữa, liệu pháp WJ-MSC đã làm tăng đáng kể sự biểu hiện của collagen loại II so với ESWT và ESWT kết hợp với WJ-MSC ở khớp gối thoái hóa. Trong phân tích các yếu tố cơ học, tác dụng hiệp đồng đã được quan sát bởi ESWT kết hợp với WJ-MSC trong biểu hiện của RUNX-2, SOX-9 và collagen Xα1 trên viêm khớp gối [21].
Người ta đã quan sát thấy rằng các exosome có nguồn gốc từ IPFP-MSC đã bảo vệ mô sụn khớp khỏi bị tổn thương và cải thiện sự bất thường về dáng đi ở chuột viêm khớp trong khi vẫn giữ cân bằng nội mô sụn, một cơ chế có thể liên quan đến sự hạn chế do miR100-5p điều chỉnh của con đường mTOR-autophagy. Wu và cộng sự đã nghiên cứu vai trò và cơ chế cơ bản của các exosome có nguồn gốc từ IPFP-MSC trên viêm khớp in vitro và in vivo. Vào thời điểm đó (2019), các tác giả đó đã tuyên bố rằng exosome có nguồn gốc từ IPFP-MSC có thể có ích trong điều trị viêm khớp gối, do trong thực hành lâm sàng tương đối dễ dàng để lấy IPFP của người từ bệnh nhân viêm khớp bằng phẫu thuật nội soi [22] .
Một nghiên cứu cho thấy rằng việc tiêm MSC từ cuống rốn người thể hiện khả năng tự sửa chữa sụn do miR-140-5p gây ra ở viêm khớp chuột, làm nổi bật công dụng điều trị tiềm năng của các mũi tiêm như vậy trong điều trị viêm khớp [23]. Trong một nghiên cứu khác về chuột bạch tạng đực trưởng thành, người ta đã quan sát thấy rằng các MSC từ cuống rốn người được tiêm vào khớp đã chữa khỏi bệnh viêm khớp gối tốt hơn so với khi chúng được tiêm vào tĩnh mạch [24].
Trong một mô hình viêm khớp ở chuột, người ta đã phát hiện ra rằng việc sử dụng có chọn lọc kartogenin đối với các MSC có nguồn gốc từ dịch khớp (SF-MSC) bằng các exosome được thiết kế đã tạo ra sự phân tán đồng đều của kartogenin trong tế bào chất, làm tăng nồng độ hiệu quả của nó trong tế bào và thúc đẩy mạnh mẽ quá trình tạo sụn của SF-MSC in vitro và in vivo [25]. Sử dụng mô hình chuột mắc viêm khớp, các tác giả khác đã quan sát thấy rằng các exosome từ MSC tủy xương người (BM-MSC) có tác động điều trị tốt đối với viêm khớp bằng cách làm giảm quá trình lão hóa và cái chết của tế bào sụn. Kết quả này gợi ý rằng các exosome có nguồn gốc từ MSC có thể có giá trị điều trị trong viêm khớp [26].
Trong mô hình viêm khớp gối chuột, người ta đã chứng minh rằng siêu âm xung cường độ thấp (LIPUS) đã cải thiện hiệu quả điều trị của MSC trong tái tạo sụn bằng cách tăng giải phóng exosome qua trung gian quá trình tự thực [27]. Trong các MSC được phân lập từ tủy xương chuột trong ống nghiệm, kết quả cho thấy LIPUS tạo điều kiện giải phóng exosome khỏi MSC bằng cách kích hoạt quá trình tự thực. Kết quả in vivo cho thấy LIPUS tăng cường đáng kể tác động tích cực của MSC trong mô sụn viêm khớp. Tác động này đã giảm đáng kể bởi GW4869, một chất ức chế giải phóng exosome [27].
Trong một mô hình viêm khớp ở chuột, các ADSC của chuột được lấy từ mô mỡ và được thay thế bằng RNA đã biến đổi. Kết quả phân tích mô học và hóa mô miễn dịch của khớp gối được thu hoạch vào lúc 4 và 8 tuần sau khi gây viêm khớp cho thấy rằng các tế bào gốc có nguồn gốc từ mô mỡ (ADSCs) phóng thích IGF-1 có hiệu quả điều trị tốt hơn so với các tế bào gốc ADSC tự nhiên. Kết quả này được thể hiện bằng điểm số quốc tế của Hiệp hội nghiên cứu xương khớp mô học thấp hơn và mất ECM ít hơn. Những kết quả như vậy đã hỗ trợ khả năng điều trị tiềm năng của IGF-1-ADSC trong điều trị viêm khớp và sửa chữa sụn trong thực hành lâm sàng [28].
Trong một nghiên cứu, các khiếm khuyết sụn khớp đã được tạo ra trong rãnh gian cốt của sụn khớp ở xương đùi thỏ. Integrin α10-MSC được dán nhãn bằng các hạt nano SPIO đồng liên hợp với rhodamine B để cho phép hiển thị bằng cả kính hiển vi MRI và huỳnh quang. Kết quả cho thấy sự di chuyển và định cư của các MSC được chọn lọc bởi integrin α10β1 của con người đối với các khiếm khuyết sụn ở đầu gối thỏ sau khi tiêm nội khớp, cũng như sự biệt hóa sụn của các MSC trong mô sụn tái tạo [29].
Trong 1 bài công bố gần đây đã đánh giá hiệu quả của việc quản lý BM-MSC trong sửa chữa sụn, sử dụng một thí nghiệm trên chuột mắc OA do monoiodoacetate gây ra ở khớp gối. Viêm khớp được gây ra ở khớp gối của chuột bằng cách tiêm monoiodoacetate (2 mg/50 µL) vào trong nang ở ngày 0. Các tác giả kết luận rằng BM-MSC có thể là một phương pháp điều trị hiệu quả cho đầu gối bị viêm và tác dụng của chúng có thể được điều hòa bởi khả năng chống viêm và chống oxy hóa của chúng [30].
Ai và cộng sự phát hiện ra rằng MSC và MSC-EV làm giảm đau viêm khớp thông qua tác động trực tiếp lên các tế bào thần kinh cảm giác ngoại biên [31]. Trong nghiên cứu của mình, các tác giả đã điều trị viêm khớp gối ở chuột C57BL/6J đực trưởng thành bằng phẫu thuật DMM. Những con chuột DMM được điều trị bằng MSC và MSC-EV không cho thấy những thay đổi hành vi liên quan đến cơn đau (ví dụ: vận động, đào và ngủ) mà những con chuột DMM không được điều trị mắc phải. Việc thiếu các hành vi liên quan đến cơn đau ở chuột được điều trị bằng MSC/MSC-EV không phải do tổn thương khớp giảm đi, mà là do khả năng giảm kích thích tế bào thần kinh cảm giác chi phối đầu gối đã được quan sát thấy ở chuột DMM không được điều trị. Hơn nữa, họ phát hiện ra rằng khả năng bị kích thích quá mức của tế bào thần kinh cảm giác do NGF gây ra đã được ngăn chặn bằng cách quản lý MSC-EV [31].
Trong một mô hình tiền lâm sàng chuyển tiếp meniscal trung gian của viêm khớp, vi nang sodium alginate của các MSC của con người đã điều chỉnh phản ứng truyền tín hiệu paracrine và cải thiện hiệu quả của điều trị viêm khớp. Ba tuần sau phẫu thuật, sau khi viêm khớp được thiết lập, các mũi hMSC được đóng gói hoặc hMSC không đóng gói được tiêm vào trong khớp. Sáu tuần sau phẫu thuật, những thay đổi vi cấu trúc ở khớp gối được định lượng bằng chụp cắt lớp vi tính. Các hMSC được bao bọc làm giảm thoái hóa sụn khớp và tái tạo xương dưới sụn [32].
Trong một đánh giá có hệ thống về các mô hình động vật và liều lượng tế bào, người ta đã quan sát thấy rằng chuột là loài được sử dụng thường xuyên nhất để mô hình hóa bệnh viêm khớp gối và việc cắt bỏ dây chằng chéo trước là phương pháp thường xuyên nhất được sử dụng để tạo ra bệnh viêm khớp [33]. Một mối tương quan đã được tìm thấy giữa liều lượng tế bào và trọng lượng cơ thể của động vật. Trong các thử nghiệm lâm sàng, có sự khác biệt lớn về liều lượng MSC được sử dụng để quản lý viêm khớp gối, từ 1 × 106 đến 200 × 106 tế bào, với mức trung bình là 37,91 × 106 tế bào. Người ta cũng phát hiện ra rằng trong các nghiên cứu tiền lâm sàng và lâm sàng về viêm khớp gối, MSC có tiềm năng đáng kể trong việc giảm đau và bảo vệ mô [33].
- Các nghiên cứu lâm sàng
- Đánh giá có hệ thống
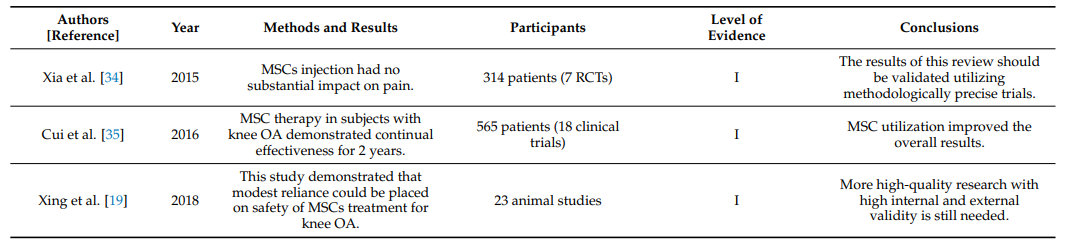
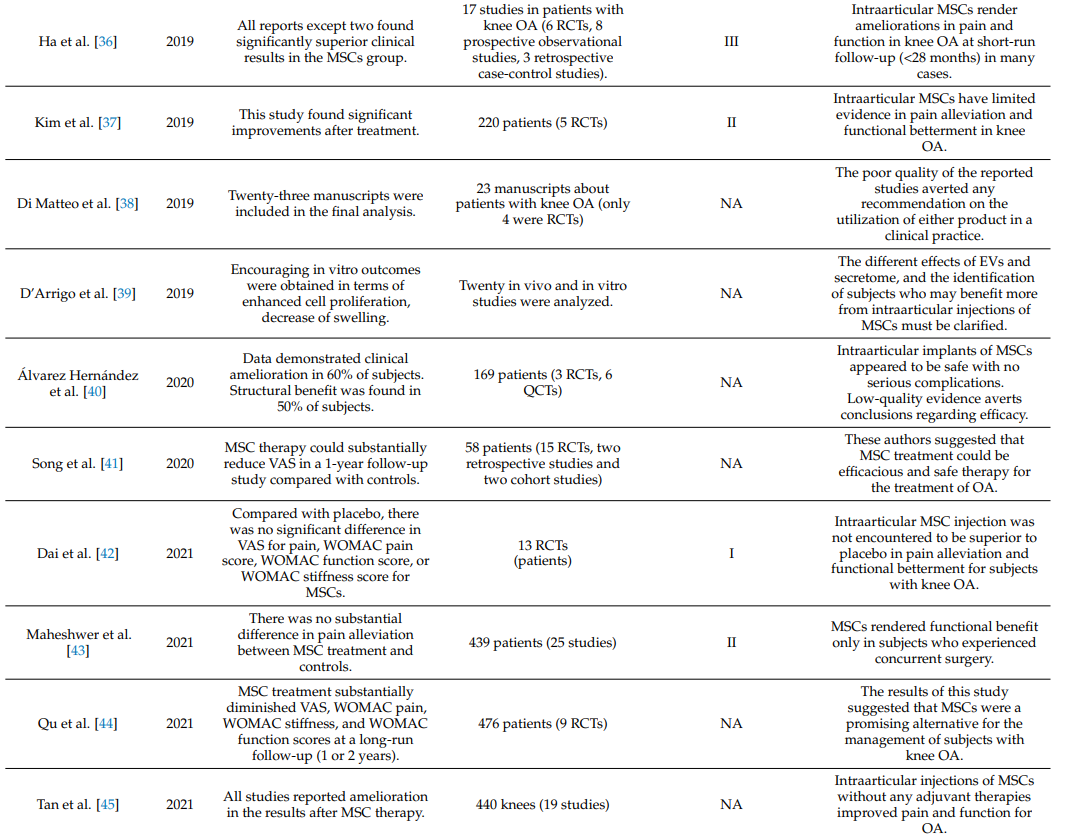
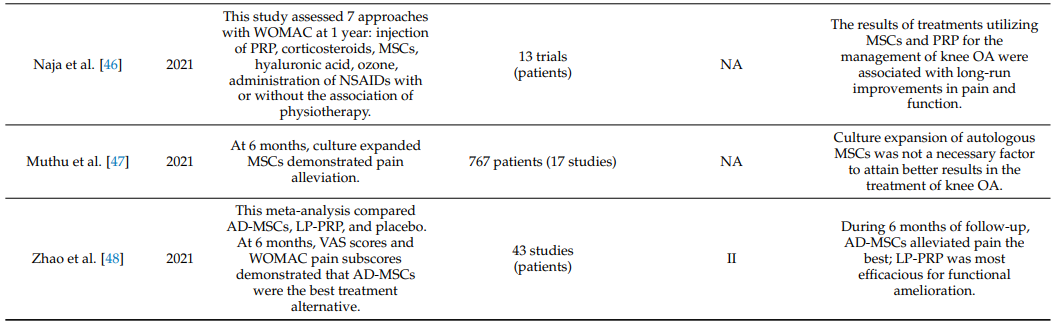
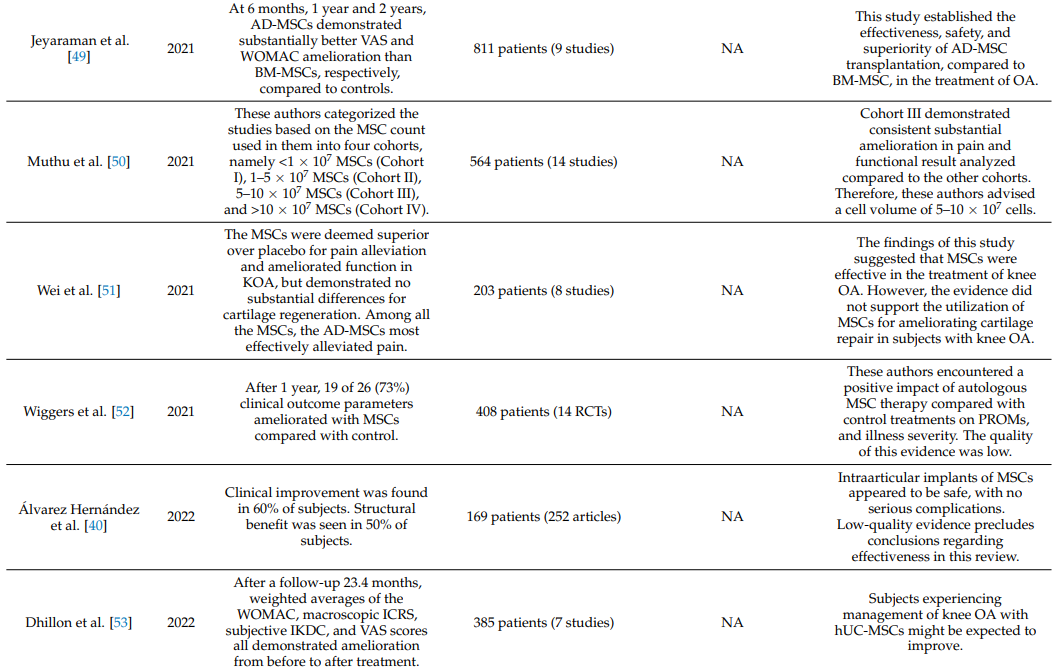
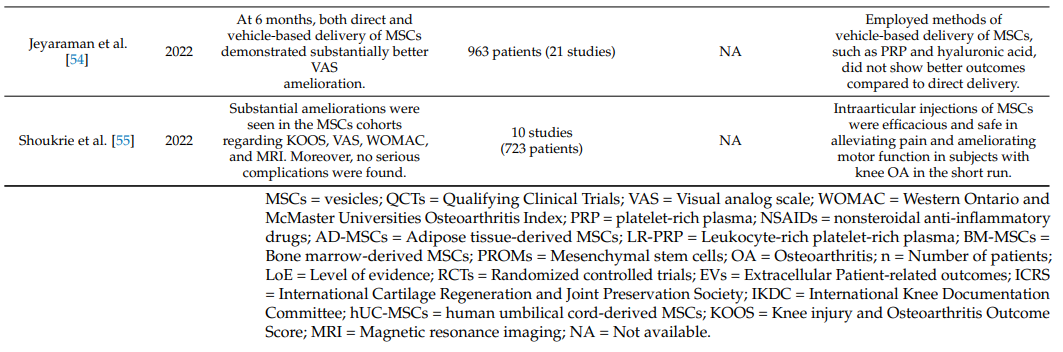
Bảng 1 tóm tắt các tổng quan hệ thống và phân tích tổng hợp về hiệu quả lâm sàng của việc tiêm MSC nội khớp trong viêm khớp gối [19,34–55].
Bảng 1. Tổng quan hệ thống và phân tích tổng hợp về hiệu quả của tiêm MSC nội khớp trong viêm khớp gối.
- Thử nghiệm ngẫu nhiên có kiểm soát (RCT)
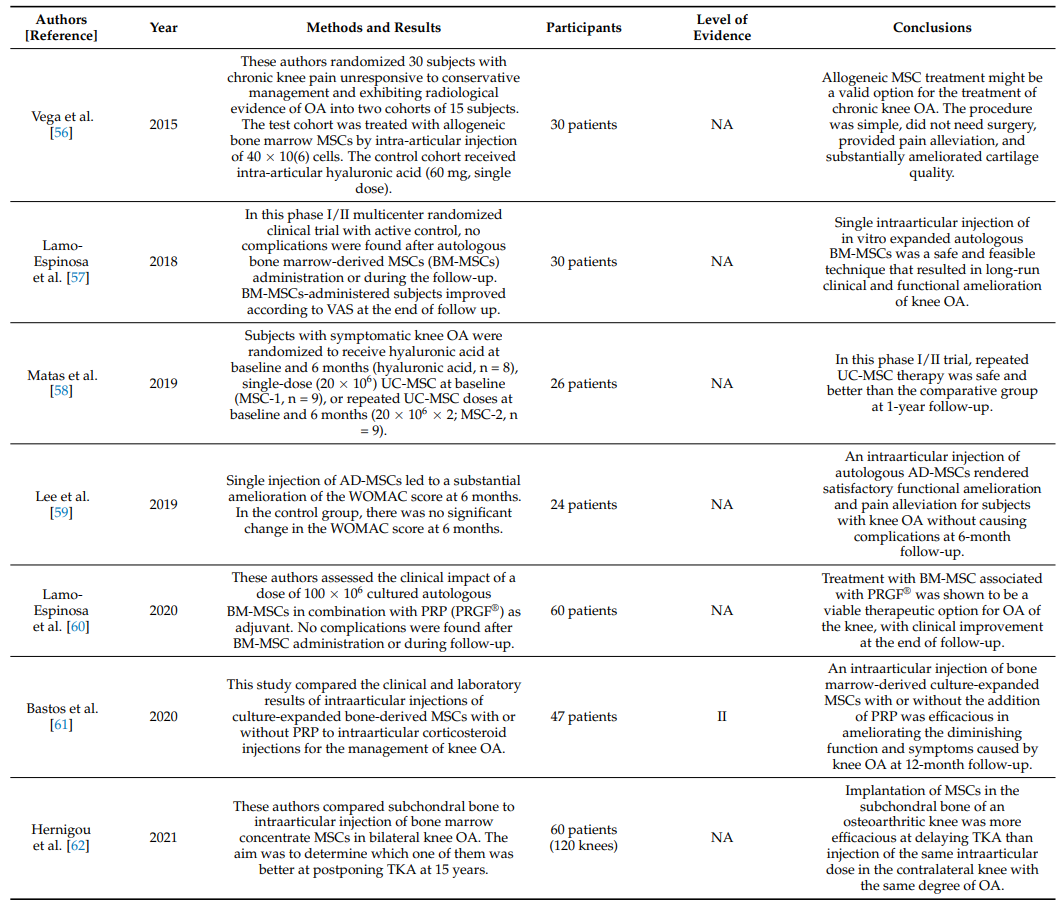
Bảng 2 tóm tắt các RCT về hiệu quả lâm sàng của việc tiêm MSC trong khớp ở bệnh nhân viêm khớp gối [56–62].
Bảng 2. Các thử nghiệm lâm sàng ngẫu nhiên (RCT) về hiệu quả của việc tiêm MSC nội khớp trong viêm khớp gối.
- Thảo luận
Quy trình của một thử nghiệm có đối chứng giả dược ngẫu nhiên đang diễn ra (thử nghiệm SCUlpTOR) nhằm mục đích đánh giá hiệu quả và hiệu quả chi phí của việc tiêm MSC trong khớp liên quan đến việc giảm đau khớp và cải thiện cấu trúc ở những người bị viêm khớp gối tibiofemoral (số đăng ký thử nghiệm: Úc New Zealand Clinical Trials Registry [ACTRN1262620000870954]; U1111-1234-4897). Các kết quả trong tương lai của thử nghiệm này sẽ giúp ích đáng kể trong việc xác định hiệu quả và tối ưu chi phí của việc tiêm MSC nội khớp trong viêm khớp gối [63].
Mục tiêu của điều trị MSC trong viêm khớp gối là toàn diện, với mục đích đạt được sự phục hồi của tất cả các thành phần khớp bị suy yếu. Tác động cận tiết của bộ gen bí mật của MSC là nền tảng cho khả năng tái tạo của các tế bào này. Việc kích hoạt các MSC đặc hiệu cho khớp gối cục bộ tạo ra một tác nhân kích thích điều hòa miễn dịch, chống dị hóa, chống apoptotic và chondrogenic [64].
Các nghiên cứu tiền lâm sàng đã chỉ ra tác động làm thay đổi triệu chứng và bệnh tật của việc điều trị bằng MSC. Trong thực hành lâm sàng, có bằng chứng cho thấy điều trị bằng MSC tự thân và đồng loại dẫn đến cải thiện đáng kể các triệu chứng và kết quả chức năng. Tuy nhiên, có những kết quả lâm sàng mâu thuẫn trong tài liệu. Mặc dù liệu pháp MSC đã mang lại kết quả đầy hứa hẹn nhưng hiệu quả của nó vẫn chưa rõ ràng. Sự đa dạng về nguồn gốc tế bào, tách chiết, phương pháp nuôi cấy và các hoàn cảnh khác khiến việc so sánh các nghiên cứu trở nên khó khăn. Cấy ghép lâm sàng về tác động điều trị bệnh của chúng vẫn chưa đạt được [64].
Gần đây, một công cụ phân tử có thể dự đoán tác động của vi môi trường khớp xương đối với việc sửa chữa sụn đã được nghiên cứu [65]. Với mục đích này, 6 chất xúc tiến khác nhau (hIL6, hIL8, hADAMTS5, hWISP1, hMMP13 và hADAM28) đã được tạo ra trong mô hình nuôi cấy viên 3 chiều và được kích thích bằng môi trường điều hòa viêm khớp (OAs-cm) thu được từ 32 bệnh nhân bị đau đầu gối viêm khớp. Sự hình thành sụn được đánh giá về mặt mô học và bằng cách định lượng sự hình thành glycosaminoglycan sunfat. Các tác giả đã chứng minh rằng OAs-cm từ các bệnh nhân khác nhau có tác dụng khác nhau đáng kể đối với sự hình thành glycosaminoglycan sunfat. Hơn nữa, họ đã quan sát thấy mối tương quan đáng kể giữa tác động của OAs-cm và sản xuất sụn và kết quả của người báo cáo quảng bá. Tính hữu ích dự đoán của việc đo lường 2 người báo cáo quảng bá với một nhóm OAs-cm độc lập đã được xác nhận. Công cụ mới này có thể dự đoán tác động của 87,5% môi trường vi mô khớp OAs-cm đối với quá trình sản xuất sụn dựa trên MSC. Đây là bước đầu tiên có liên quan đối với các phương pháp sửa chữa sụn được cá nhân hóa cho bệnh nhân viêm khớp, cho phép dự đoán liệu vi môi trường khớp viêm khớp có cho phép sửa chữa sụn hay không; do đó, nó có thể có tầm quan trọng lớn trong việc xác định sự thành công của các chiến lược sửa chữa sụn sử dụng MSC [65].
Có một số yếu tố chính có thể ảnh hưởng đến hiệu quả của việc tiêm MSC trong khớp, chẳng hạn như tế bào đồng loại so với tế bào tự thân, tế bào sơ cấp so với tế bào nuôi cấy, tế bào biệt hóa so với tế bào không biệt hóa, tế bào được cấp phép so với tế bào không được cấp phép, sự biến đổi của các chế phẩm tế bào và điều kiện lâm sàng của người nhận.
Đối với các MSC đồng loại so với tự thân, các nguy cơ và hạn chế có thể xảy ra khi sử dụng các MSC tự thân so với đồng loại trong thực hành lâm sàng vẫn đang được tranh luận, chẳng hạn như ảnh hưởng có thể có của sự không đồng nhất của người hiến tặng. Hình 3 cho thấy những ưu điểm và nhược điểm được báo cáo của các MSC đồng loại và tự thân trong thực hành lâm sàng và tiền lâm sàng [66].

Liên quan đến các MSC sơ cấp so với các tế bào nuôi cấy, chất nền ngoại bào tủy xương tự nhiên tạo ra một môi trường vi mô duy nhất làm giảm sự phát triển của MSC trong môi trường không có huyết thanh và duy trì chất lượng của MSC về mặt sao chép, biệt hóa và đáp ứng protein-2 hình thái xương. Việc sử dụng một hệ thống nuôi cấy mạnh bao gồm ECM đặc hiệu cho mô bản địa và môi trường không có huyết thanh xác định sẽ cho phép chúng tôi chuẩn bị một lượng đáng kể MSC đồng thời duy trì các đặc tính tế bào gốc của chúng cho các phương pháp điều trị dựa trên tế bào [67].
Xét về các MSC biệt hóa so với các MSC không biệt hóa, một nghiên cứu đã so sánh kết quả của việc ghép các ADSC không biệt hóa vào tủy sống bị dập của chuột so với các ADSC được tạo ra bởi hai phương pháp khác nhau để tạo ra mô thần kinh biệt hóa. Những phát hiện của nghiên cứu này cho thấy rằng các ADSC có thể biệt hóa thành các tế bào giống như tế bào thần kinh trong ống nghiệm và trong cơ thể sống. Tuy nhiên, các ADSC biệt hóa thần kinh không dẫn đến phục hồi chức năng tốt hơn so với các ADSC không biệt hóa [68].
Liên quan đến các MSC được cấp phép so với các MSC không được cấp phép, việc cấp phép in vitro trước khi áp dụng điều trị có thể dẫn đến phản ứng điều hòa miễn dịch và điều trị có thể thấy trước hơn đối với việc điều trị MSC so với việc cấp phép viêm nhiễm in vivo bởi môi trường người nhận [69]. Một số tác giả đưa ra bằng chứng mạnh mẽ về việc sử dụng cấp phép TGF-β1 như một cách tiếp cận độc đáo để cải thiện khả năng ức chế miễn dịch của MSC [70]. Vào năm 2021, Lu và Qiao tuyên bố rằng, mặc dù có sự không đồng nhất, nhưng việc cấp phép trước không ảnh hưởng đến chu kỳ tế bào và tính chất của các MSC có nguồn gốc từ tủy xương của con người. Hiệu lực tạo xương đã giảm và hiệu lực chondrogenic được tăng lên, trong khi hiệu lực tạo mỡ ổn định trong các MSC được cấp phép. Các MSC được cấp phép cũng thể hiện khả năng điều hòa miễn dịch hiệu quả hơn, bao gồm biểu hiện của các chemokine, cytokine, phân tử bề mặt và thụ thể có liên quan [71].
Đối với sự thay đổi trong quá trình chuẩn bị tế bào, exosome được giải phóng bởi MSC đã được coi là ứng cử viên tốt cho chấn thương sụn và quản lý viêm khớp, và exosome cho thực hành lâm sàng cần được sản xuất quy mô lớn. Để đạt được mục tiêu này, các MSC chất lỏng hoạt dịch của con người đã được phát triển trên các hạt chất mang siêu nhỏ và sau đó được nuôi cấy trong một hệ thống nuôi cấy 3 chiều năng động. Hệ thống nuôi cấy này đã thu được thành công các exosome quy mô lớn từ các chất nổi trên bề mặt nuôi cấy MSC của chất lỏng hoạt dịch, cho thấy rằng kỹ thuật này có thể tạo ra một lượng lớn các exosome cấp thực hành sản xuất tốt. Những exosome này có thể được sử dụng trong nghiên cứu sinh học exosome và quản lý viêm khớp lâm sàng [72]. Trong một nghiên cứu, các vi cầu alginate-gelatin nhúng ADSC có thể tiêm được điều chế bằng phương pháp phun điện. So với các kính hiển vi alginate truyền thống, khả năng hỗ trợ của nó đối với ADSC tốt hơn và thể hiện hiệu quả sửa chữa tốt hơn. Cách tiếp cận này có thể hữu ích cho việc tái tạo mô sụn [73].
Liên quan đến các điều kiện lâm sàng của người nhận, đã có báo cáo rằng 40 × 106 MSC có nhiều khả năng đạt được các phản ứng tối ưu nhất ở những bệnh nhân bị viêm khớp gối cấp độ 2. Mặc dù những cải thiện đáng kể đã được tìm thấy khi sử dụng số lượng tế bào kém hơn (24 × 106) và cao hơn (100 × 106), chúng vẫn gây ra đau và viêm dai dẳng [12].
Hiệu quả của việc tiêm MSC trong khớp đối với bệnh viêm khớp gối vẫn còn gây tranh cãi, mặc dù hầu hết các ấn phẩm gần đây đều cho thấy tác dụng giảm đau trong thời gian ngắn. Các bác sĩ phẫu thuật chỉnh hình quản lý bệnh nhân bị viêm khớp gối ngày càng quan tâm đến MSC, mặc dù thông tin lâm sàng và dữ liệu khoa học cơ bản là thiếu quyết đoán. Cần có thêm nghiên cứu so sánh MSC với giả dược.
Cần có một quy trình chuẩn cho việc tiêm MSC trong khớp ở bệnh nhân viêm khớp gối. Quy trình này phải bao gồm những điều sau: lựa chọn tế bào, xác thực (phân tích kiểu hình và khả năng biệt hóa đa năng, đặc biệt là biệt hóa với các tế bào tiền thân), kỹ thuật nuôi cấy hoặc tăng sinh, liều lượng và chương trình phục hồi chức năng sau khi điều trị [74].
Hạn chế chính của đánh giá này là việc lựa chọn các bài báo được phân tích cuối cùng là chủ quan, tức là những bài báo mà chúng tôi cho là có liên quan trực tiếp nhất đến tiêu đề của bài báo. Vì vậy, có thể là một số bài báo quan trọng đã không được đưa vào. Bài viết này không phải là một đánh giá có hệ thống về tài liệu, mà là một đánh giá tường thuật về các bài báo mà chúng tôi thấy có liên quan nhất.
- Kết luận
Gần đây đã có nhiều cuộc điều tra về tiêm MSC nội khớp để quản lý viêm khớp gối. Mặc dù phần lớn các báo cáo gần đây cho rằng tiêm MSC nội khớp làm giảm đau đầu gối trong thời gian ngắn, nhưng hiệu quả của chúng vẫn còn gây tranh cãi, do dữ liệu khoa học hiện tại về MSC là thiếu quyết đoán. Trước khi tư vấn tiêm MSC nội khớp thường xuyên ở những bệnh nhân bị viêm khớp gối đau, cần có thêm nghiên cứu so sánh MSC với giả dược, cũng như một quy trình chuẩn để tiêm MSC nội khớp ở bệnh nhân viêm khớp gối.
Nguồn: Tạp chí Quốc tế về Khoa học Phân tử
Link: https://pubmed.ncbi.nlm.nih.gov/36499280/