Diseases, 08/01/2026
Giới thiệu
Ở những bệnh nhân được mở xương ức đường giữa, đặc biệt sau bắc cầu động mạch vành (CABG), nhiễm trùng sâu vết mổ xương ức (DSWI) có thể tiến triển thành viêm xương ức mạn tính – một biến chứng lâm sàng nghiêm trọng. Tỷ lệ DSWI sau mở xương ức dao động từ 0,25–5%. Mặc dù được điều trị kịp thời và toàn diện, tỷ lệ tử vong vẫn ở mức cao đáng báo động; các tổng quan hệ thống và phân tích gộp cho thấy DSWI có thể chiếm tới khoảng một nửa số ca tử vong nội viện, trở thành một trong những biến chứng đe dọa tính mạng nhất của phẫu thuật tim.
Tế bào gốc trung mô (MSCs) được xem là một hướng tiếp cận đầy tiềm năng trong điều trị các nhiễm trùng mạn tính, bao gồm DSWI. Secretome của MSCs có đặc tính kháng khuẩn nổi bật nhờ tiết các peptide kháng khuẩn như LL-37 – có khả năng phá hủy trực tiếp màng vi khuẩn đồng thời điều hòa miễn dịch mạnh mẽ thông qua “tái lập trình” các tế bào miễn dịch tại chỗ, đặc biệt là đại thực bào. Sự hoạt hóa này thúc đẩy chuyển đổi kiểu hình từ M1 tiền viêm sang M2 kháng viêm và thực bào, qua đó tăng thải trừ vi khuẩn và hạn chế tình trạng viêm mạn tính phá hủy mô. Ngoài ra, các chiết xuất từ MSCs thể hiện tiềm năng tái tạo cao trong liền thương da thông qua nhiều cơ chế, bao gồm tái hoạt hóa nguyên bào sợi trung bì. Bản thân MSCs cũng có thể biệt hóa thành mô liên kết, thay thế các tế bào tổn thương tại vị trí vết thương, đồng thời thúc đẩy tân sinh mạch và tăng di cư tế bào đến vùng tổn thương.
Tuy nhiên, không phải mọi nguồn MSCs đều có hiệu quả và năng lực tái tạo tương đương. MSCs nguồn chu sinh (thu từ các mô bao quanh thai nhi) có nhiều ưu thế so với MSCs trưởng thành, bao gồm mức độ “non” cao hơn, khả năng tăng sinh mạnh hơn và tính sinh miễn dịch thấp hơn. Đáng chú ý, chúng có xu hướng tiền u thấp hoặc thậm chí thể hiện hoạt tính kháng u. Hơn nữa, các MSCs này được thu nhận từ những nguồn sinh học thường bị loại bỏ sau sinh như nước ối, nhau thai và dây rốn, do đó hầu như không bị hạn chế về vấn đề đạo đức.
Wharton’s jelly (WJ) – thành phần của dây rốn – là một nguồn dồi dào MSCs chưa trưởng thành. MSCs từ Wharton’s jelly (WJ-MSCs) được đánh giá cao trong y học tái tạo nhờ khả năng điều hòa cận tiết mạnh thông qua tiết nhiều yếu tố có hoạt tính sinh học. WJ-MSCs đã được chứng minh thúc đẩy tăng sinh biểu mô và tăng tốc quá trình liền thương, với hiệu quả ghi nhận ở các vết thương da sâu và vết thương nhiễm trùng sau bỏng nặng. Tuy nhiên, việc ứng dụng trực tiếp WJ-MSCs trên lâm sàng vẫn còn hạn chế, và về hiệu quả tái tạo mô, đặc biệt trong các vết thương phẫu thuật nhiễm trùng mạn tính ở người cao tuổi – nhóm có khả năng sửa chữa mô suy giảm, vẫn còn thiếu dữ liệu.
Trong báo cáo này, chúng tôi trình bày một trường hợp nam bệnh nhân cao tuổi được chẩn đoán viêm xương ức mạn tính kháng trị và viêm trung thất sau CABG. Sự tồn tại của vết thương mạn tính không liền kèm theo nhiễm COVID-19 trong giai đoạn quanh phẫu thuật đã đòi hỏi điều chỉnh chiến lược điều trị theo hướng cá thể hóa, đa giai đoạn nhằm tối ưu hóa hiệu quả lâm sàng.
Báo cáo ca lâm sàng
Bệnh nhân nam, 63 tuổi, lần đầu bị nhồi máu cơ tim cấp vào năm 2014 và được đặt stent động mạch vành theo chiến lược can thiệp phân kỳ. Năm 2016, bệnh nhân tái xuất hiện cơn đau thắt ngực nặng. Kết quả chụp mạch vành kiểm tra cho thấy tổn thương đa nhánh động mạch vành. Tháng 12/2016, bệnh nhân được phẫu thuật bắc cầu động mạch vành (CABG) trong điều kiện không sử dụng tuần hoàn ngoài cơ thể (off-pump). Phẫu thuật bao gồm bắc cầu động mạch ngực trong – động mạch liên thất trước, cùng với bắc cầu tự thân bằng tĩnh mạch hiển lớn (vena saphena magna) cho nhánh chéo, nhánh bờ tù của động mạch mũ và động mạch mũ.
Khoảng ba tuần sau CABG (đầu năm 2017), bệnh nhân xuất hiện tình trạng chảy mủ tại 1/3 dưới sẹo mổ xương ức (Hình 1A). Trong các năm 2017, 2018 và 2020, bệnh nhân được phẫu thuật cắt bỏ đường rò thêm ba lần. Tuy nhiên, tình trạng viêm kéo dài, tái phát đường rò và chậm liền vết thương vẫn tồn tại mặc dù đã điều trị kháng sinh theo kháng sinh đồ do nhiễm Staphylococcus aureus (≈10⁵ CFU/mL), sử dụng Cefuroxime (0,75 g mỗi 8 giờ), sau đó chuyển sang Ceftriaxone (2 g mỗi 12 giờ).
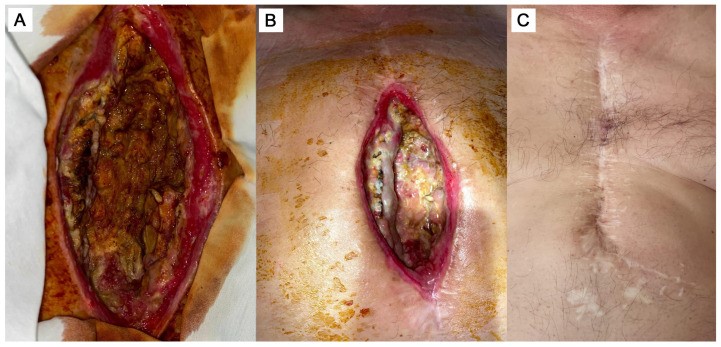
Hình 1. Tình trạng vết mổ trước điều trị (A); sau 6 ngày kể từ khi bắt đầu liệu pháp tế bào bổ trợ phẫu thuật (B) và sau 4 năm theo dõi (C).
Ngày 11/5/2021, bệnh nhân được phẫu thuật lại do tình trạng đáp ứng viêm hệ thống gia tăng rõ rệt (CRP = 168,46 mg/L; presepsin = 351 pg/mL; bạch cầu = 18,7 × 10⁹/L). Đường rò xuyên qua xương ức, lan vào khoang màng tim và thất phải, đã được cắt bỏ. Tuy nhiên, trong hai tuần tiếp theo, tình trạng liền vết thương kém và dấu hiệu viêm mạn tính vẫn tiếp diễn.
Ngày 27/5/2021, sau khi có sự đồng thuận tham gia điều trị, bệnh nhân được tiêm thấm quanh bờ vết thương một chế phẩm tế bào đồng loài chứa MSCs và nguyên bào sợi. Nguồn tế bào được thu nhận từ dây rốn do một cơ sở sản khoa cung cấp (không phải sản phẩm thương mại). Chế phẩm có nồng độ 1 × 10⁶ tế bào/mL trong dung dịch NaCl 0,9%. Quy trình tiêm được thực hiện bằng bơm tiêm insulin vô khuẩn 1,0 mL với kim nhỏ nhằm đảm bảo liều chính xác và hạn chế tổn thương mô quanh vết thương. Thuốc được tiêm nội bì và tiêm dưới da dọc theo chu vi vết thương, cách bờ tổn thương 0,5–1,0 cm. Quy trình được lặp lại 3 lần, mỗi 48 giờ (ngày 1, 3 và 5), nhằm duy trì hiệu quả điều trị.
Kỹ thuật tiêm tạo sẩn da bằng cách bơm 0,1–0,2 mL mỗi điểm, khoảng cách giữa các điểm tiêm 1 cm, tổng cộng 10–15 mũi tiêm quanh đường rò nhằm kích thích tân sinh mạch và thúc đẩy biểu mô hóa bờ vết thương trước khi tiến hành tạo hình lồng ngực theo kế hoạch.
Trong những ngày sau đó, ghi nhận cải thiện rõ rệt tại chỗ: ngừng tiết dịch bệnh lý và tiến triển liền thương (Hình 1B).
Trong giai đoạn chuẩn bị phẫu thuật tiếp theo, xét nghiệm sàng lọc phát hiện RNA SARS-CoV-2; bệnh nhân không có triệu chứng và tình trạng này không ảnh hưởng đáng kể đến quá trình liền vết thương. Trước và sau phẫu thuật tái tạo, bệnh nhân được điều trị kháng sinh toàn thân bằng piperacillin + tazobactam (4,5 g mỗi 8 giờ).
Ngày 12/7/2021, khám tại chỗ cho thấy vết thương vẫn còn hở; các chỉ số viêm hệ thống vẫn cao (CRP = 130,88 mg/L; tốc độ lắng máu = 63 mm/h). Siêu âm tim ghi nhận phân suất tống máu thất trái (LVEF) giảm còn 49–50% và có dấu hiệu phình thất trái.
Ngày 16/7/2021, bệnh nhân được phẫu thuật tái tạo cuối cùng gồm: kết hợp xương ức bằng nẹp kim loại, ghép xương tự thân vùng mào chậu và cố định lại các xương sườn vào xương ức. Tại thời điểm can thiệp, đáy vết thương có mô hạt tốt, không còn dịch bệnh lý. Các bờ xương ức và xương sườn 5–7 được bóc tách để tạo điều kiện tái tạo cấu trúc; mảnh ghép xương tự thân được cố định vào khuyết xương ức bằng hai nẹp kim loại và neo vào khớp sụn các xương sườn liên quan.
Sau phẫu thuật, tình trạng viêm giảm dần (CRP còn 47,31 mg/L vào ngày 27/7/2021). Dẫn lưu sau xương ức được rút ngày 19/7/2021. Siêu âm tim kiểm tra ngày 22/7/2021 cho thấy LVEF giảm xuống 39%; tuy nhiên, bệnh nhân vẫn ổn định huyết động, không có sung huyết hay phù ngoại vi. Suy tim được kiểm soát hiệu quả theo phác đồ chuẩn với thuốc chẹn beta (bisoprolol), ức chế men chuyển (lisinopril) và kháng aldosterone. Bệnh nhân xuất viện ngày 2/8/2021 sau 21 ngày điều trị nội trú, trong tình trạng ổn định.
Sau xuất viện, bệnh nhân được theo dõi ngoại trú. Xương ức vững chắc, vết thương liền kỳ đầu. Tình trạng toàn thân cải thiện, các dấu hiệu viêm tại chỗ giảm rõ; bạch cầu và CRP dần trở về gần mức bình thường (sau 1 tháng: CRP = 15,15 mg/L; bạch cầu = 10,66 × 10⁹/L). Trong theo dõi dài hạn, vết thương đóng kín hoàn toàn và mô tái tạo đầy đủ. Hình 1C minh họa tình trạng vết mổ khoảng 4 năm sau liệu pháp tế bào.
Thảo luận
Các kết quả thực nghiệm trong thập kỷ qua cho thấy các mô chu sinh ở người như nhau thai, màng ối, dây rốn, cũng như các dịch chu sinh gồm dịch ối và máu dây rốn, chứa nhiều quần thể tế bào tiền thân đa năng. Những tế bào này được gọi chung là tế bào gốc trung mô chu sinh (P-MSCs), có ý nghĩa đặc biệt trong y học tái tạo nhờ sở hữu nhiều ưu thế so với các MSCs nguồn “trưởng thành” (A-MSCs), điển hình như từ tủy xương (BM-MSCs) hoặc mô mỡ (AD-MSCs).
Thứ nhất, P-MSCs có tiềm năng tái tạo cao do kiểu hình còn non và tính gốc cao hơn. Đây là yếu tố quan trọng trong ứng dụng lâm sàng, khi hiệu quả điều trị thường đòi hỏi số lượng tế bào lên đến hàng trăm triệu.
Thứ hai, P-MSCs có tính sinh miễn dịch thấp; nhiều trường hợp ghép đồng loài thành công mà không xảy ra thải ghép đã được ghi nhận. Chúng biểu hiện rất thấp phân tử phức hợp hòa hợp mô chính lớp I (MHC I), hầu như không biểu hiện MHC II và các phân tử đồng kích thích như CD80, CD86. Đặc tính “ưu thế miễn dịch” này cho phép sử dụng trong bối cảnh ghép đồng loài mà không cần yêu cầu tương hợp kháng nguyên bạch cầu người (HLA) nghiêm ngặt.
Thứ ba, P-MSCs có nguy cơ sinh u thấp, thậm chí có thể thể hiện đặc tính kháng u. So với A-MSCs, chúng tích lũy ít đột biến di truyền hơn, do đó giảm nguy cơ chuyển dạng ác tính trong điều kiện nuôi cấy in vitro.
Cuối cùng, các mô chu sinh như dây rốn và nhau thai thường bị loại bỏ sau sinh như chất thải y tế. Vì vậy, việc thu nhận nguồn tế bào này an toàn, dễ tiếp cận và không xâm lấn đến người hiến. Khác với MSCs đồng loài từ nguồn trưởng thành, đòi hỏi quy trình can thiệp xâm lấn; hoặc tế bào gốc phôi liên quan đến nhiều tranh luận đạo đức, việc thu thập mô chu sinh hầu như không đặt ra vấn đề đạo đức.
Tế bào gốc trung mô từ Wharton’s jelly (WJ-MSCs) là một phân nhóm MSCs có nguồn gốc từ mô chu sinh. Wharton’s jelly là một dạng mô liên kết đặc biệt bao quanh các mạch máu dây rốn, có chức năng bảo vệ cơ học (Hình 2A), đồng thời là một “kho dự trữ” tế bào gốc quan trọng và được xem như nguồn tiêu chuẩn tham chiếu của các P-MSCs.
Khi nuôi cấy in vitro, WJ-MSCs có hình thái nguyên bào sợi điển hình (Hình 2B) và biểu hiện các dấu ấn bề mặt theo tiêu chuẩn của Hiệp hội Quốc tế về Liệu pháp Tế bào và Gen (ISCT): dương tính với CD90, CD105 và CD73; âm tính với các dấu ấn huyết học như CD45 và CD34.
WJ-MSCs có tốc độ tăng sinh cao trong điều kiện nuôi cấy, cho phép thu nhận số lượng tế bào đạt ngưỡng điều trị từ một mẫu hiến duy nhất trong thời gian tương đối ngắn. Về tiềm năng biệt hóa, chúng có khả năng chuyển dạng in vitro thành sụn (chondrocytes), xương (osteocytes) và mỡ (adipocytes).
Đặc tính điều hòa miễn dịch được xem là lợi thế điều trị nổi bật nhất của WJ-MSCs. Không chỉ có tính “ưu thế miễn dịch”, chúng còn chủ động điều chỉnh đáp ứng miễn dịch bằng cách ức chế tăng sinh tế bào T, đồng thời điều hòa hoạt động của tế bào B, tế bào tua (dendritic cells) và tế bào NK, qua đó tạo môi trường kháng viêm mạnh mẽ.
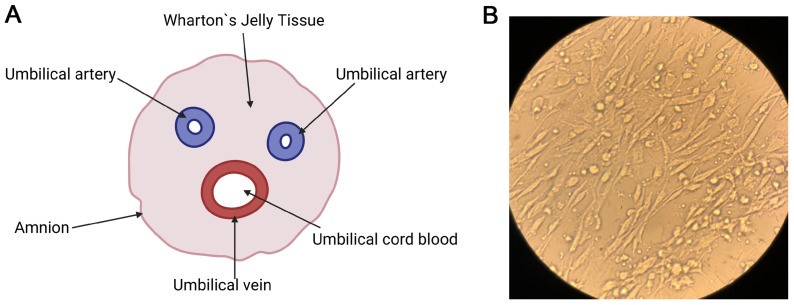
Hình 2. Tế bào gốc trung mô từ Wharton’s jelly (WJ-MSCs). (A) Sơ đồ cắt ngang dây rốn người, minh họa các cấu trúc giải phẫu chính: màng ối bên ngoài (amnion) bao quanh mô Wharton’s jelly (mô liên kết nhầy); thành phần mạch máu gồm hai động mạch rốn và một tĩnh mạch rốn chứa máu dây rốn. (B) Hình thái WJ-MSCs nuôi cấy in vitro.
Việc chuyển giao lâm sàng liệu pháp MSC trong điều trị vết thương mạn tính, nhiễm trùng xương hoặc đau mạn tính nhìn chung cho kết quả không đồng nhất. Một thử nghiệm lâm sàng ngẫu nhiên mù đôi quy mô lớn trên 114 bệnh nhân đau thắt lưng mạn tính (so sánh BM-MSC đồng loài với giả dược) không đạt được tiêu chí chính sau 12 tháng theo dõi. Tổng quan 449 thử nghiệm MSC trong lĩnh vực chấn thương chỉnh hình (đến tháng 12/2023) cho thấy chỉ 12,5% công bố kết quả được bình duyệt; hơn một nửa đề cương không nêu rõ nồng độ tế bào tiêm. Những bất nhất phương pháp luận này cản trở khả năng so sánh, tái lập và phát triển MSC thành sản phẩm điều trị chuẩn hóa.
Tuy vậy, một phân tích gộp trên hơn 30 nghiên cứu với khoảng 2500 bệnh nhân xác nhận MSC có hiệu quả trong đóng kín vết thương, tái tạo mô và tân sinh mạch, trong đó chủ yếu sử dụng MSC nguồn trưởng thành (tủy xương và mô mỡ).
MSC trưởng thành, đặc biệt BM-MSC, tồn tại nhiều hạn chế. Lấy tủy xương từ mào chậu là thủ thuật xâm lấn, gây đau và tiềm ẩn nguy cơ nhiễm trùng. Quan trọng hơn, tỷ lệ MSC trong tủy xương rất thấp (0,001–0,01% tế bào đơn nhân), tương đương 60–600 tế bào/mL dịch hút, khiến việc sử dụng trực tiếp không khả thi và đòi hỏi tăng sinh ex vivo kéo dài, làm phát sinh hiện tượng lão hóa in vitro. Bên cạnh đó, lão hóa sinh học in vivo là giới hạn nền tảng: khả năng tăng sinh và sinh xương của BM-MSC giảm rõ theo tuổi; ở người trên 60 tuổi, biểu hiện mRNA phosphatase kiềm (dấu ấn sinh xương chủ chốt) giảm gấp ba lần so với nhóm dưới 50 tuổi. Do đó, nghịch lý điều trị xuất hiện: liệu pháp tự thân bằng MSC trưởng thành lại kém hiệu quả nhất ở nhóm bệnh nhân cao tuổi – những người cần điều trị nhất.
Ngược lại, MSC chu sinh như WJ-MSC không mang các hạn chế này. Trong mô hình chuột, WJ-MSC thúc đẩy hình thành xương vượt trội so với BM-MSC (62,5% so với 25%), cho thấy tiềm năng tham gia tái tạo xương ức. Nghiên cứu in vivo cũng chứng minh tính sống còn cao và ưu thế sinh xương rõ rệt của WJ-MSC. Ngoài ra, WJ-MSC hoặc secretome của chúng đã được chứng minh hiệu quả trong các vết thương mạn tính khó liền như loét dinh dưỡng; việc bôi tại chỗ secretome/exosome giúp rút ngắn thời gian hồi phục loét đái tháo đường. Tiêm thấm WJ-MSC quanh vết thương có thể điều hòa đáp ứng viêm tại chỗ, giảm tải vi sinh và thúc đẩy hình thành mô hạt đầy đủ, tạo điều kiện thuận lợi cho tạo hình lồng ngực và phục hồi cấu trúc xương ức.
Tổng hợp các ưu điểm của WJ-MSC, thu nhận không xâm lấn, khả năng tăng sinh cao, không phụ thuộc tuổi người hiến, hoạt tính sinh xương nổi bật và hiệu quả trong liền thương là cơ sở lựa chọn WJ-MSC trong ca lâm sàng này. Kết quả cho thấy WJ-MSC có thể là liệu pháp bổ trợ tiềm năng cho phẫu thuật chỉnh sửa truyền thống, đặc biệt ở bệnh nhân nguy cơ cao. Mục tiêu lâm sàng kỳ vọng bao gồm liền thương hoàn toàn, ổn định thành ngực và không tái phát nhiễm trùng, kể cả ở người cao tuổi.
Tuy nhiên, báo cáo này còn nhiều hạn chế. Thứ nhất, thiếu các nghiên cứu đối chứng độc lập hoặc đa trung tâm về WJ-MSC trong vết thương xương ức mạn tính, nên chưa thể khẳng định chắc chắn hiệu quả quan sát được hoàn toàn do liệu pháp tế bào. Thứ hai, sử dụng tế bào đồng loài luôn tiềm ẩn nguy cơ phản ứng miễn dịch. Trong ca bệnh này, WJ-MSC không biểu hiện HLA-DR (≤2% tế bào dương tính), phù hợp với mức nền và cho thấy nguy cơ hoạt hóa miễn dịch thấp. Tuy vậy, ở các bệnh cảnh tự miễn hoặc suy giảm miễn dịch, cần đánh giá thận trọng nguy cơ miễn dịch, đặc biệt nếu sử dụng đường toàn thân. Do đó, cần thêm các nghiên cứu quy mô lớn nhằm xác định đầy đủ tính an toàn dài hạn và hồ sơ biến cố bất lợi của liệu pháp WJ-MSC.
Kết luận
Báo cáo ca bệnh này cho thấy tế bào gốc trung mô Wharton’s jelly đồng loài (WJ-MSCs) có thể thúc đẩy quá trình liền vết thương xương ức sau phẫu thuật bắc cầu động mạch vành (CABG). Trong trường hợp của chúng tôi, việc sử dụng WJ-MSCs đã góp phần thay đổi diễn tiến của viêm xương ức mạn tính kháng trị ở một bệnh nhân cao tuổi nguy cơ cao, đồng thời có tình trạng dương tính với COVID-19.
Chiến lược điều trị hai giai đoạn, bao gồm cắt lọc triệt để ổ nhiễm trùng và tiếp theo là liệu pháp WJ-MSCs, không chỉ kiểm soát và chấm dứt quá trình viêm mạn tính mà còn thúc đẩy đáng kể các quá trình tái tạo tại vùng tổn thương. Kinh nghiệm lâm sàng của chúng tôi cho thấy WJ-MSCs có tiềm năng mang lại lợi ích điều trị trong các trường hợp nhiễm trùng sâu vết mổ xương ức phức tạp.
Việc ứng dụng WJ-MSCs có thể được xem xét mở rộng trong thực hành lâm sàng như một chiến lược an toàn và hiệu quả. Tuy nhiên, cần thêm các nghiên cứu tiến cứu và các loạt ca bệnh với quy mô lớn hơn nhằm xác định rõ chỉ định, tối ưu hóa phác đồ sử dụng và xác nhận hiệu quả dài hạn, từ đó từng bước tích hợp phương pháp này vào tiêu chuẩn điều trị phẫu thuật chuyên sâu hiện đại.
Tài liệu tham khảo
Ganina, A., Baigenzhin, A., Chuvakova, E., Yerzhigit, N., Zhunussov, A., Akhayeva, A., Kozina, L., Lookin, O., & Askarov, M. (2026). Intradermal Application of Allogenic Wharton’s Jelly Mesenchymal Stem Cells for Chronic Post-Thoracotomy Wound in an Elderly Patient After Coronary Artery Bypass Grafting: Clinical Case with Brief Literature Review. Diseases (Basel, Switzerland), 14(1), 27.
Nguồn: Diseases