Journal of Translational Medicine, 11/06/2025
Giới thiệu
Thoái hóa khớp gối (Osteoarthritis – OA) là bệnh lý mạn tính thường gặp nhất trong các bệnh khớp, gây tổn thương sụn, xương dưới sụn và màng hoạt dịch. OA gây đau, hạn chế vận động, và là nguyên nhân hàng đầu gây tàn tật ở người trung niên và cao tuổi. Theo thống kê toàn cầu, hơn 27 triệu người Mỹ mắc OA, và chi phí y tế hằng năm vượt 180 tỷ USD. Hiện nay, các biện pháp điều trị chủ yếu (giảm đau, kháng viêm, tiêm nội khớp hoặc thay khớp) chỉ giúp giảm triệu chứng mà chưa phục hồi được mô sụn bị tổn thương.
Trong thập kỷ qua, liệu pháp tế bào gốc trung mô (MSCs) đã mở ra hướng mới trong điều trị OA. MSCs có khả năng biệt hóa, chống viêm, điều hòa miễn dịch và tái tạo mô. Tuy nhiên, việc sử dụng trực tiếp MSCs còn nhiều hạn chế: khó kiểm soát khả năng sống sót, nguy cơ hình thành khối u hoặc phản ứng miễn dịch. Các bằng chứng mới cho thấy exosome – túi ngoại bào nhỏ do MSCs tiết ra – là yếu tố chính trung gian tác dụng của MSCs. Exosome có kích thước nano (50–150 nm), chứa protein, RNA, microRNA và lipid điều hòa quá trình viêm và tái tạo mô. So với tế bào gốc, exosome ổn định hơn, ít gây thải ghép và dễ bảo quản, vận chuyển.
Đặc biệt, exosome từ tế bào gốc trung mô dây rốn người (hUC-MSC-Exos) được xem là nguồn hiệu quả và an toàn nhất vì dây rốn là mô thừa sau sinh, ít vấn đề đạo đức, và tế bào có khả năng tăng sinh mạnh. Các nghiên cứu tiền lâm sàng đã chứng minh hUC-MSC-Exos có thể:
- Giảm tiết các yếu tố viêm như IL-6, TNF-α, MMP13;
- Tăng biểu hiện collagen type II và aggrecan trong tế bào sụn (chondrocyte);
- Ức chế con đường NF-κB, AKT, và MAPK;
- Thúc đẩy tái tạo sụn và giảm tổn thương xương dưới sụn.
Tuy vậy, chưa có nhiều bằng chứng lâm sàng xác nhận tính an toàn và hiệu quả của việc tiêm exosome ở người. Do đó, nhóm tác giả thực hiện nghiên cứu này nhằm đánh giá tác dụng của hUC-MSC-Exos từ giai đoạn tiền lâm sàng đến thử nghiệm lâm sàng, để xác định tiềm năng điều trị OA.
Phương pháp
Nguồn và đặc tính của tế bào gốc trung mô từ dây rốn (hUC-MSCs)
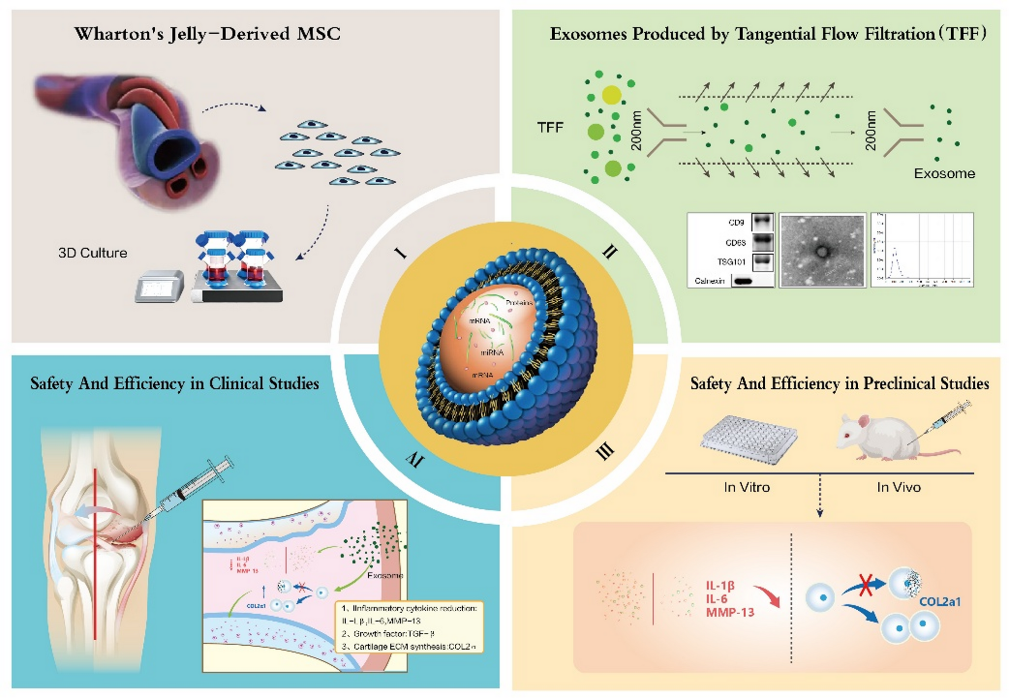
Tế bào gốc trung mô được tách từ phần Wharton’s jelly của dây rốn người hiến khỏe mạnh sau sinh, theo quy trình được phê duyệt đạo đức y khoa. Mẫu dây rốn được rửa sạch bằng dung dịch PBS có bổ sung penicillin/streptomycin để loại bỏ máu và cặn. Mô được cắt nhỏ, tiêu hóa bằng collagenase type I và trypsin, sau đó nuôi trong môi trường DMEM/F12 có bổ sung 10% huyết thanh thai bò (FBS). Các tế bào được nuôi ở 37 °C, 5% CO₂, và thay môi trường mỗi 3 ngày. Khi đạt 80–90% mật độ, tế bào được chuyền sang bình mới (passage 3–5) để đảm bảo tính ổn định.
Đặc tính của hUC-MSCs được xác nhận bằng:
- Xét nghiệm hình thái học: tế bào hình thoi, sắp xếp xoáy như nguyên bào sợi.
- Định danh marker bề mặt (flow cytometry): dương tính với CD73, CD90, CD105; âm tính với CD34, CD45, HLA-DR.
- Khả năng biệt hóa đa dòng: biệt hóa thành tế bào mỡ, xương và sụn trong môi trường cảm ứng tương ứng, xác nhận bằng nhuộm Oil Red O, Alizarin Red và Alcian Blue.
Tách và định danh exosome từ hUC-MSCs
Exosome (hUC-MSC-Exos) được thu từ dịch nuôi cấy MSCs sau 48 giờ trong môi trường không chứa FBS. Dịch thu được được xử lý theo quy trình ly tâm tầng:
Lần 1: 300 × g trong 10 phút → loại bỏ tế bào sống.
Lần 2: 2.000 × g trong 20 phút → loại bỏ mảnh vụn tế bào.
Lần 3: 10.000 × g trong 30 phút → loại bỏ vi hạt lớn.
Lần 4: 100.000 × g trong 70 phút (ultracentrifugation) → thu kết tủa chứa exosome. Kết tủa được rửa lại trong PBS và tái ly tâm 100.000 × g để tinh sạch, sau đó bảo quản ở −80 °C.
Đặc tính của exosome được xác nhận bằng ba kỹ thuật:
- Kính hiển vi điện tử truyền qua (TEM): quan sát hình cầu, màng kép, kích thước 80–150 nm.
- Phân tích kích thước hạt (Nanoparticle Tracking Analysis, NTA): đường kính trung bình 100 ± 20 nm.
- Western blot: xác nhận các protein đặc trưng CD9, CD63, TSG101, và âm tính với calnexin (marker nội bào, kiểm soát tạp).
Thí nghiệm in vitro trên tế bào sụn (chondrocyte)
Tế bào sụn khớp chuột được kích thích bằng IL-1β (10 ng/mL) để mô phỏng tình trạng viêm trong OA. Sau đó, các nhóm được xử lý bằng hUC-MSC-Exos ở các nồng độ khác nhau (10, 50, 100 µg/mL).
Đánh giá:
- Biểu hiện gen và protein viêm (IL-6, TNF-α, MMP13) bằng RT-qPCR và Western blot.
- Đánh giá gen tổng hợp sụn (COL2A1, aggrecan) để xác định khả năng bảo vệ mô sụn.
- Phân tích hình thái học dưới kính hiển vi huỳnh quang để xác định mức độ thoái hóa tế bào sụn.
Mô hình động vật (in vivo)
Mô hình OA được tạo ra ở chuột bằng cách tiêm enzyme collagenase vào khớp gối để gây thoái hóa sụn. Sau 7 ngày, các con chuột được chia ngẫu nhiên thành 3 nhóm:
Nhóm 1: Nhóm chứng (PBS)
Nhóm 2: Nhóm Exo-thấp (10 µg exosome/khớp)
Nhóm 3: Nhóm Exo-cao (50 µg exosome/khớp)
Tiêm nội khớp 1 lần/tuần trong 4 tuần. Sau điều trị, khớp gối được thu mẫu và đánh giá:
- Nhuộm HE và Safranin O/Fast Green đánh giá cấu trúc sụn.
- Tính điểm OARSI (Osteoarthritis Research Society International) để định lượng mức tổn thương.
- Phân tích mô học màng hoạt dịch để đánh giá phản ứng viêm.
Thử nghiệm lâm sàng giai đoạn đầu
Thiết kế và đối tượng nghiên cứu
Thử nghiệm lâm sàng giai đoạn I/IIa được thiết kế ngẫu nhiên, mù đôi, tăng liều, có nhóm chứng, nhằm đánh giá độ an toàn và hiệu quả ban đầu của hUC-MSC-Exos trong điều trị thoái hóa khớp gối.
- Đối tượng: 36 bệnh nhân OA độ II–III theo phân loại Kellgren–Lawrence.
- Tiêu chuẩn loại trừ: có bệnh lý khớp khác, nhiễm trùng khớp, rối loạn đông máu, hoặc bệnh tự miễn.
- Phân nhóm:
- Liều thấp: 50 µg exosome/khớp
- Liều trung bình: 100 µg/khớp
- Liều cao: 200 µg/khớp
- Nhóm chứng: dung dịch đệm PBS
Exosome được tiêm vào khoang khớp gối bằng kim nhỏ vô trùng, 1 lần/tháng × 3 tháng.
Theo dõi và đánh giá
- Thời gian theo dõi: 12 tuần sau mũi tiêm cuối.
- Đánh giá lâm sàng:
- Thang WOMAC (Western Ontario and McMaster Universities Osteoarthritis Index): đánh giá mức độ đau, độ cứng, và chức năng vận động.
- Thang VAS (Visual Analogue Scale): cường độ đau chủ quan.
- Đánh giá hình ảnh: MRI khớp gối để phân tích độ dày sụn, phù tủy xương, và tình trạng màng hoạt dịch.
- Theo dõi an toàn: công thức máu, chức năng gan thận, CRP, dấu hiệu phản ứng tại chỗ, và các tác dụng phụ hệ thống.
Tất cả bệnh nhân được theo dõi chặt chẽ trong 24 giờ đầu sau tiêm để phát hiện sớm phản ứng tức thì, và tiếp tục được kiểm tra định kỳ trong suốt 3 tháng.
Kết quả
Tiền lâm sàng:
- hUC-MSCs biệt hóa tốt thành tế bào xương, mỡ và sụn, xác nhận đặc tính MSC.
- Exosome thu được có kích thước trung bình ~100 nm, hình cầu màng kép, biểu hiện rõ các marker CD9, CD63, TSG101.
- Trên tế bào sụn của chuột bị viêm, hUC-MSC-Exos giảm đáng kể biểu hiện IL-6 và MMP13, đồng thời tăng COL2A1 và aggrecan, chứng tỏ có tác dụng chống viêm và bảo vệ sụn.
- Trong mô hình chuột OA, tiêm nội khớp exosome giảm tổn thương sụn và dày màng hoạt dịch, quan sát bằng nhuộm Safranin O và điểm số OARSI.
Lâm sàng:
- Không có phản ứng bất lợi nghiêm trọng (sốc phản vệ, nhiễm trùng, viêm màng hoạt dịch).
- Một số bệnh nhân có sưng nhẹ tại chỗ tiêm nhưng tự hồi phục sau 1–2 ngày.
- Sau 12 tuần, điểm WOMAC giảm rõ rệt ở nhóm liều trung bình và cao, so với nhóm giả dược.
- Hình ảnh MRI cho thấy bề dày sụn tăng nhẹ, giảm tín hiệu phù tủy xương, cải thiện cấu trúc mô khớp.
- Không phát hiện thay đổi bất thường về men gan, creatinine, hay dấu hiệu viêm toàn thân.
Thảo luận
Nghiên cứu này là bằng chứng đầu tiên trên người cho thấy việc tiêm exosome từ hUC-MSCs an toàn và có tác dụng cải thiện triệu chứng OA.
So với các liệu pháp tế bào gốc trực tiếp, exosome mang nhiều ưu điểm:
- Không chứa nhân tế bào → không nguy cơ hình thành khối u.
- Dễ bảo quản, vận chuyển, tiêu chuẩn hóa liều lượng.
- Có thể tiêm nhiều lần mà không cần gây mê hoặc can thiệp phẫu thuật.
Cơ chế chính được đề xuất gồm:
- Điều hòa miễn dịch: exosome ức chế con đường NF-κB, giảm tiết IL-1β, TNF-α.
- Bảo vệ tế bào sụn: tăng tổng hợp collagen II và proteoglycan, ức chế enzyme phân hủy MMP13, ADAMTS5.
- Tái tạo mô: exosome chứa microRNA (miR-100-5p, miR-21, miR-140-3p…) kích hoạt tín hiệu PI3K/AKT và Wnt/β-catenin, thúc đẩy tăng sinh chondrocyte.
Các kết quả MRI và WOMAC cho thấy cải thiện rõ nhất ở nhóm liều trung bình, gợi ý có mức liều tối ưu, do liều cao hơn có thể làm bão hòa thụ thể nội bào hoặc tăng phản ứng thực bào loại bỏ exosome. Tuy nhiên, nghiên cứu cũng thừa nhận một số hạn chế:
- Cỡ mẫu lâm sàng còn nhỏ, thời gian theo dõi ngắn (12 tuần).
- Chưa đánh giá được tác dụng lâu dài lên cấu trúc sụn hoặc tiến triển OA.
- Cần phân tích sâu hơn thành phần RNA, protein trong exosome để xác định phân tử chủ chốt.
Kết luận
Exosome từ tế bào gốc trung mô dây rốn người (hUC-MSC-Exos) là liệu pháp tiềm năng, an toàn và hiệu quả bước đầu trong điều trị thoái hóa khớp gối.
Nghiên cứu này chứng minh:
- Exosome có khả năng chống viêm, bảo vệ tế bào sụn, thúc đẩy tái tạo mô khớp.
- Tiêm nội khớp hUC-MSC-Exos an toàn, không gây phản ứng bất lợi nghiêm trọng.
- Hiệu quả lâm sàng thể hiện qua cải thiện điểm WOMAC và MRI sau 12 tuần.
Nhóm nghiên cứu đề xuất thực hiện thử nghiệm đa trung tâm, cỡ mẫu lớn, theo dõi dài hạn để xác định hiệu quả bền vững và tối ưu hóa phác đồ điều trị.
Tài liệu tham khảo
Bài viết được dịch và tóm tắt từ bài báo (nếu có): Wang, Y., Kong, Y., Du, J., Qi, L., Liu, M., Xie, S., Hao, J., Li, M., Cao, S., Cui, H., Liu, A., Ma, J. & Song, Y. (2025). Injection of human umbilical cord mesenchymal stem cells exosomes for the treatment of knee osteoarthritis: from preclinical to clinical research. Journal of Translational Medicine, 23, 641.
Nguồn: Journal of Translational Medicine
Link: https://translational-medicine.biomedcentral.com/articles/10.1186/s12967-025-06623-y?utm_source=chatgpt.com#citeas