Stem Cell Res Ther, 08/01/2026
Giới thiệu
Nhồi máu cơ tim (MI) được đặc trưng bởi sự tắc nghẽn tưới máu mạch vành và giảm cung cấp oxy cho cơ tim, gây gánh nặng y tế, xã hội và kinh tế đáng kể trên toàn cầu. Việc áp dụng rộng rãi các liệu pháp tái thông mạch đã cải thiện tỷ lệ sống sót sau thiếu máu cục bộ ban đầu; tuy nhiên, tỷ lệ suy tim sau MI lại gia tăng. Tim bị nhồi máu trải qua quá trình tái cấu trúc, bao gồm mỏng không cân xứng vùng cơ tim hoại tử và phì đại vùng cơ tim không hoại tử, dẫn đến suy tim hậu MI. Các điều trị dược lý, thiết bị hỗ trợ tim và liệu pháp tái đồng bộ tim hiện nay có thể làm chậm suy giảm chức năng tim, đảo ngược tiến triển suy tim và giảm tử vong, nhưng không thể bổ sung các tế bào cơ tim đã mất. Liệu pháp tái tạo sử dụng tế bào ngoại sinh để tái sinh và sửa chữa tim thiếu máu là một chiến lược đầy hứa hẹn trong bệnh tim mạch. Mục tiêu chính của các liệu pháp dựa trên tế bào là tái tạo cơ tim trực tiếp bằng tế bào ngoại sinh hoặc kích hoạt cơ chế sửa chữa nội sinh thông qua tác động cận tiết. Tuy vậy, thải ghép miễn dịch vẫn là rào cản không thể tránh khỏi, hạn chế việc ứng dụng lâm sàng các liệu pháp tái tạo này.
Các chiến lược hiện có nhằm đạt dung nạp miễn dịch gồm cảm ứng dung nạp miễn dịch trung ương và ngoại vi, sử dụng thuốc ức chế miễn dịch, các mảnh ghép tế bào được thiết kế sinh học, và tạo tế bào “phổ quát”. Những nghiên cứu gần đây cho thấy việc thiết lập dung nạp miễn dịch ngoại vi là phương pháp tiềm năng để tăng khả năng lưu giữ tế bào. Các nghiên cứu trước của chúng tôi chứng minh rằng truyền tĩnh mạch tế bào gốc trung mô người (hMSCs) giúp cải thiện khả năng bám ghép và hiệu quả điều trị của các tế bào được cấy ghép nội cơ tim và nội cơ trong mô hình MI và thiếu máu chi sau. Tuy nhiên, việc tiêm tĩnh mạch liều MSC cao không làm tăng hiệu quả điều hòa miễn dịch. Ngoài ra, kháng nguyên bạch cầu người HLA-G được ghi nhận có khả năng điều hòa miễn dịch thông qua cảm ứng tế bào T điều hòa HLA-G+ và Foxp3+, đồng thời điều chỉnh hoạt động của tế bào NK. HLA-G là phân tử then chốt trong dung nạp miễn dịch mẹ-thai và đã được bàn luận rộng rãi trong ghép tạng đặc. Tuy nhiên, việc tăng biểu hiện HLA-G có thể cải thiện thêm khả năng sống sót và hiệu quả điều trị của liệu pháp tế bào hay không vẫn chưa rõ.
Trong nghiên cứu gần đây của chúng tôi, các tế bào MSC có nguồn gốc từ máu dây rốn người biểu hiện quá mức HLA-G1 đã được tạo thành công. Do đó, nghiên cứu này giả thuyết rằng, so với hUCB-MSCs thông thường, việc truyền tĩnh mạch toàn thân hUCB-MSCs tăng biểu hiện HLA-G1 có thể tăng khả năng lưu giữ tế bào và cải thiện hiệu quả điều trị của tế bào cơ tim có nguồn gốc từ tế bào gốc đa năng cảm ứng người (hiPSC-CMs) được cấy nội cơ tim trong mô hình chuột MI. Đồng thời, cơ chế nền tảng của tác dụng điều hòa miễn dịch từ MSCs tăng biểu hiện HLA-G1 cũng được khảo sát.
Phương pháp
Nuôi cấy và chuẩn bị hUCB-MSCs và hiPSC-CMs
hUCB-MSCs được tinh sạch, định danh bằng marker đặc trưng, chọn các tế bào có khả năng biệt hóa đa dòng và sử dụng ở passage 4–6; sau đó được tiêm tĩnh mạch ở chuột. hiPSC-CMs có nhịp đập được xác nhận đặc tính cơ tim bằng nhuộm miễn dịch và flow cytometry (≈95% cTnT dương tính), được đánh dấu DiR trước khi cấy ghép nội cơ tim.
Chuyển nạp HLA-G1 người
hUCB-MSCs được chuyển nạp lentivirus có hoặc không mang gen HLA-G1 để tạo dòng tăng biểu hiện. Tế bào được chia thành ba nhóm: MSC nguyên bản, MSC-NC (lentivirus gắn GFP đối chứng), và MSC-HLA-G1 (lentivirus tăng biểu hiện HLA-G1). Hiệu quả chuyển nạp được xác nhận sau nuôi cấy bằng qRT-PCR và western blot, cho thấy HLA-G1 được tăng biểu hiện thành công.
Thiết lập mô hình nhồi máu cơ tim chuột, phân nhóm và theo dõi tế bào
Chuột ICR được sử dụng để đánh giá tác dụng kháng viêm của MSCs. Trước khi gây nhồi máu cơ tim cấp (AMI) 1 tuần, chuột được tiêm tĩnh mạch dung dịch muối, hUCB-MSCs hoặc hUCB-MSCs tăng biểu hiện HLA-G1. AMI được tạo bằng thắt động mạch vành liên thất trước trái dưới gây mê; điện tâm đồ dùng để xác nhận mô hình. Sau 30 phút, chuột được tiêm nội cơ tim môi trường nuôi cấy hoặc hiPSC-CMs đã đánh dấu DiR tại vùng rìa ổ nhồi máu; kháng sinh được dùng dự phòng nhiễm trùng. Những con chết trong thủ thuật bị loại khỏi phân tích.
Tổng cộng 30 chuột được chia ngẫu nhiên thành 5 nhóm: Sham, AMI, AMI + CM, MSC + AMI + CM, và HLA-G1 MSC + AMI + CM. Sau 28 ngày, chức năng tim được đánh giá bằng siêu âm tim, sau đó động vật được gây mê quá liều để thu thập tim và các cơ quan nhằm kiểm tra hình thành khối u. Khả năng lưu giữ tế bào được theo dõi vào ngày 7 và 28 bằng hệ thống chụp ảnh huỳnh quang IVIS, dựa trên tín hiệu của tế bào hiPSC-CMs gắn DiR.
Khảo sát siêu âm tim
Vào ngày 28, chức năng tim của chuột AMI được đánh giá bằng siêu âm tim qua thành ngực sử dụng hệ thống FUJIFILM Visual Sonics với đầu dò 10 S-RS. Chuột được gây mê bằng việc cho hít isoflurane và duy trì nhịp tim 500–600 bpm. Việc đo được thực hiện bởi kỹ thuật viên giàu kinh nghiệm theo khuyến cáo của Hiệp hội Tim mạch Châu Âu. Chuột được đặt ở tư thế nằm nghiêng trái, thu nhận hình ảnh cạnh ức của thất trái và sử dụng mặt cắt trục dài để phân tích chức năng tim.
Chức năng tim được đánh giá bằng các thông số M-mode tiêu chuẩn gồm đường kính cuối tâm thu thất trái (LVESD), đường kính cuối tâm trương thất trái (LVEDD), phân suất co rút (FS) và phân suất tống máu thất trái (LVEF). Giá trị trung bình của ba chu kỳ tim cho mỗi con vật được tính bởi chuyên gia đánh giá mù với thí nghiệm.
Đánh giá mô học
Sau khi động vật hi sinh, tim được thu thập để đánh giá mô học. Mô được cố định trong đệm formalin 4%, khử nước theo thang ethanol, đúc paraffin và cắt lát dày 5 µm. Nhuộm H&E được thực hiện bằng bộ kit thương mại. Nhuộm Masson Trichrome được dùng để đánh giá kích thước vùng nhồi máu; diện tích nhồi máu được tính bằng tỷ lệ mô xơ nhuộm xanh so với tổng diện tích thất trái, đo trên ba lát cắt và lấy giá trị trung bình.
Apoptosis tại vùng rìa nhồi máu được đánh giá bằng nhuộm TUNEL. Tân sinh mạch được khảo sát bằng nhuộm huỳnh quang miễn dịch với α-SMA và vWF, mật độ mạch được tính theo số mạch dương tính trên mỗi mm². Dữ liệu được thu từ 6 trường nhìn ngẫu nhiên (40×) trên ba lát cắt, theo quy trình đánh giá mù, và được ghi nhận bằng hệ thống kính hiển vi tự động.
Phân tích flow cytometry
Tế bào lách được thu sau khi động vật hi sinh để phân tích flow cytometry. Sau khi loại bỏ hồng cầu, huyền phù tế bào đơn được chuẩn bị trong PBS. Khoảng 1 × 10⁶ tế bào được ủ chặn với kháng thể kháng CD16/32 và 7AAD trong dung dịch đệm flow.
Các quần thể tế bào T và NK được nhuộm bằng các kháng thể đặc hiệu để xác định T CD3+, CD4+, CD8+ và tế bào NK. Tế bào T điều hòa (Treg) được nhuộm bằng bộ kit chuyên dụng gồm CD4, CD25 và Foxp3. Mẫu được phân tích trên máy flow cytometer CytoFLEX, sử dụng đối chứng FMO cho chiến lược gating đa màu, và xử lý dữ liệu bằng phần mềm FlowJo.
Biến đổi các cytokine
Các tế bào lách CD4+ được đồng nuôi cấy in vitro với hUCB-MSCs hoặc hUCB-MSCs tăng biểu hiện HLA-G1 nhằm đánh giá tác dụng điều hòa miễn dịch. Tế bào CD4+ được tách bằng nhuộm kháng thể anti-CD4-FITC và tuyển chọn bằng FACS. Sau đó, 5 × 10⁵ tế bào CD4+ được đồng nuôi cấy với 1 × 10⁵ MSCs trong hệ thống transwell trong 7 ngày. Dịch nổi nuôi cấy được thu thập để định lượng cytokine bằng bộ assay đa chỉ tiêu theo hướng dẫn của nhà sản xuất.
Phân tích thống kê
Dữ liệu được xử lý bằng SPSS 27.0, trình bày dưới dạng trung bình ± SEM. So sánh nhiều nhóm bằng ANOVA một yếu tố kèm kiểm định Tukey; p < 0,05 được xem là có ý nghĩa thống kê.
Kết quả
35 con chuột được gây nhồi máu cơ tim, trong đó 5 con tử vong, còn 30 con được đưa vào phân tích và chia ngẫu nhiên thành 5 nhóm. hUCB-MSCs biểu hiện các marker đặc trưng MSC và không biểu hiện marker tạo máu. Việc chuyển nạp lentivirus thành công, và nhóm MSC-HLA-G1 cho thấy tăng biểu hiện HLA-G1 rõ rệt so với các nhóm đối chứng.
hiPSC-CMs được xác nhận đặc tính cơ tim bằng nhuộm miễn dịch và flow cytometry (~95% cTnT dương tính). Không ghi nhận hình thành khối u tại vị trí tiêm hoặc các cơ quan. Điện tâm đồ cho thấy đoạn ST chênh lên, xác nhận mô hình nhồi máu cơ tim được tạo thành công.
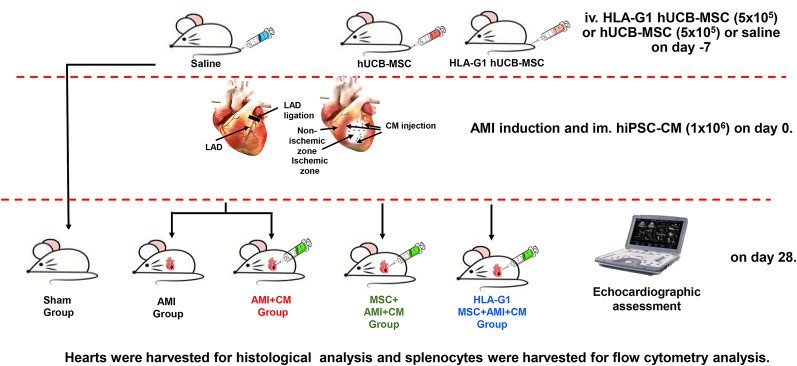
Hình 1. Sơ đồ quy trình thí nghiệm
Tác dụng điều hòa miễn dịch của hUCB-MSCs và hUCB-MSCs tăng biểu hiện HLA-G1
Phân tích flow cytometry tế bào lách cho thấy không có khác biệt giữa các nhóm Sham, AMI và AMI + CM. Tuy nhiên, truyền tĩnh mạch hUCB-MSCs hoặc hUCB-MSCs tăng biểu hiện HLA-G1 làm tăng rõ rệt tỷ lệ Treg ở lách so với nhóm AMI, trong đó nhóm MSC-HLA-G1 tăng mạnh hơn so với MSC thường. Ngược lại, AMI làm tăng tế bào NK ở lách, và ghép hiPSC-CMs không ảnh hưởng đến chỉ số này; truyền MSCs làm giảm NK, trong đó MSC-HLA-G1 cho hiệu quả giảm mạnh hơn. Không ghi nhận thay đổi đáng kể ở quần thể CD4+ T.
Trong thí nghiệm đồng nuôi cấy in vitro, hUCB-MSCs làm giảm các cytokine tiền viêm (IFN-γ, TNF-α, IL-2, IL-17A) nhưng không làm thay đổi cytokine kháng viêm; hiệu quả ức chế cytokine tiền viêm rõ hơn khi dùng MSCs tăng biểu hiện HLA-G1. Kết quả cho thấy MSCs tăng biểu hiện HLA-G1 tạo tác dụng điều hòa miễn dịch mạnh hơn MSCs thường, ít nhất một phần thông qua việc giảm tiết cytokine tiền viêm.
Tăng khả năng bám ghép và lưu giữ tế bào sau cấy ghép
Chụp huỳnh quang vào ngày 7 và 28 cho thấy truyền tĩnh mạch hUCB-MSCs hoặc hUCB-MSCs tăng biểu hiện HLA-G1 làm tăng đáng kể khả năng bám ghép và lưu giữ hiPSC-CMs tại vùng rìa ổ nhồi máu so với nhóm chỉ ghép tế bào. Hiệu quả này rõ hơn ở nhóm MSC tăng biểu hiện HLA-G1 so với MSC thường, và duy trì đến ngày 28.
Kết quả cho thấy MSCs truyền tĩnh mạch giúp cải thiện sự tồn tại của hiPSC-CMs ghép nội cơ tim, phù hợp với các nghiên cứu trước. MSCs tăng biểu hiện HLA-G1 tạo hiệu ứng mạnh hơn, gợi ý vai trò tăng cường điều hòa miễn dịch trong việc nâng cao lưu giữ tế bào ghép.
Giảm kích thước vùng nhồi máu và tỷ lệ apoptosis sau cấy ghép
Nhuộm H&E, Masson và TUNEL cho thấy nhóm AMI có vùng nhồi máu lớn và tỷ lệ apoptosis cao. Cấy ghép hiPSC-CMs làm giảm kích thước vùng nhồi máu và apoptosis ở vùng rìa ổ nhồi máu so với nhóm AMI; hiệu quả này được tăng cường khi kết hợp truyền tĩnh mạch hUCB-MSCs.
Đặc biệt, hUCB-MSCs tăng biểu hiện HLA-G1 giúp giảm thêm kích thước vùng nhồi máu và apoptosis, cho thấy tăng cường hiệu quả điều trị, phù hợp với vai trò điều hòa miễn dịch mạnh hơn của HLA-G1.
Tăng tạo mạch và tân sinh mạch
Nhuộm huỳnh quang α-SMA và vWF cho thấy AMI làm giảm mật độ mạch tại vùng rìa ổ nhồi máu. Cấy ghép hiPSC-CMs giúp cải thiện tạo mạch, và hiệu quả tăng thêm khi kết hợp truyền tĩnh mạch hUCB-MSCs. Đáng chú ý, MSCs tăng biểu hiện HLA-G1 tiếp tục làm tăng mạnh hơn quá trình tạo mạch và tân sinh mạch.
Kết quả cho thấy MSCs truyền tĩnh mạch nâng cao hiệu quả điều trị của hiPSC-CMs, trong đó MSCs tăng biểu hiện HLA-G1 cho tác dụng thúc đẩy tạo mạch vượt trội.
Cải thiện chức năng tâm thu thất trái sau cấy ghép
Siêu âm tim cho thấy AMI làm suy giảm nặng chức năng thất trái (giảm LVEF, FS và tăng LVEDD, LVESD). Cấy ghép hiPSC-CMs giúp cải thiện rõ rệt các chỉ số chức năng tim; hiệu quả tiếp tục tăng khi kết hợp truyền tĩnh mạch hUCB-MSCs.
Đáng chú ý, hUCB-MSCs tăng biểu hiện HLA-G1 cải thiện chức năng tim mạnh hơn MSCs thường, với LVEF và FS cao hơn, đồng thời LVESD giảm hơn. Kết quả cho thấy MSCs tăng biểu hiện HLA-G1 tăng cường hiệu quả phục hồi chức năng tim sau nhồi máu.
Thảo luận
Kết quả cho thấy truyền tĩnh mạch hUCB-MSCs làm tăng đáng kể khả năng bám ghép của hiPSC-CMs được cấy nội cơ tim, phù hợp với các nghiên cứu trước. hUCB-MSCs tăng biểu hiện HLA-G1 có hiệu quả điều hòa miễn dịch mạnh hơn MSCs thường. Việc giảm cytokine tiền viêm và tăng Treg ở lách giúp cải thiện điều hòa miễn dịch và tăng lưu giữ tế bào ghép, từ đó liên quan đến phục hồi chức năng tim, đi kèm với tăng tạo mạch và giảm viêm cũng như apoptosis tại vùng rìa ổ nhồi máu.
Tác dụng điều hòa miễn dịch của hUCB-MSCs tăng biểu hiện HLA-G1
Các nghiên cứu trước của chúng tôi cho thấy tiêm tĩnh mạch 5 × 10⁵ MSCs làm tăng đáng kể mức độ ghép và hiệu quả điều trị của hiPSC-CMs được cấy trong cơ tim, trong khi tăng liều MSCs không cải thiện thêm tác dụng điều hòa miễn dịch. HLA-G là một phân tử HLA lớp I không cổ điển, đóng vai trò quan trọng trong dung nạp miễn dịch mẹ–thai và thường được sử dụng để giảm viêm và tăng hiệu quả điều hòa miễn dịch trong ghép tế bào. So với MSCs từ các nguồn khác, hUCB-MSCs biểu hiện HLA-G1 cao hơn trong điều kiện nuôi cấy chuẩn. Trong nghiên cứu này, hUCB-MSCs tăng biểu hiện HLA-G1 được sử dụng nhằm tăng khả năng ghép của hiPSC-CMs. Do Treg lách đạt đỉnh 7 ngày sau truyền MSCs, chúng tôi tiêm tĩnh mạch MSCs trước ghép 7 ngày. Kết quả cho thấy MSCs tăng biểu hiện HLA-G1 cải thiện đáng kể mức độ ghép, liên quan đến tăng Treg và giảm NK lách, cho thấy giảm thải ghép qua cả cơ chế phụ thuộc và không phụ thuộc MHC.
Để đánh giá sâu hơn tác dụng điều hòa miễn dịch, các cytokine được phân tích sau 7 ngày đồng nuôi cấy MSCs với CD4⁺ splenocytes. Ngoài IFN-γ, TNF-α và IL-17A, MSCs còn làm giảm IL-2 tiền viêm. Mặc dù IL-2 thấp thường liên quan giảm Treg, trong nghiên cứu này Treg không giảm, có thể do MSCs tiết các yếu tố như IDO và HLA-G thúc đẩy tăng sinh Treg. Cả hiPSC-MSCs và hUCB-MSCs đều cho hiệu quả điều hòa miễn dịch tương tự, nhưng chưa thể kết luận loại nào ưu thế hơn.
Nhìn chung, tiêm tĩnh mạch hUCB-MSCs điều hòa đáp ứng miễn dịch bằng cách giảm cytokine tiền viêm và tế bào NK, đồng thời tăng Treg, qua đó cải thiện hiệu quả ghép hiPSC-CMs trong cơ tim.
Cơ chế cải thiện chức năng tim
Kết quả cho thấy truyền tĩnh mạch hUCB-MSCs hoặc hUCB-MSCs tăng biểu hiện HLA-G1 giúp cải thiện rõ chức năng tim sau 28 ngày nhồi máu cơ tim, trong đó nhóm HLA-G1 hiệu quả cao hơn. Hiệu quả điều trị liên quan đến giảm kích thước vùng nhồi máu, giảm apoptosis, tăng bám ghép tế bào và tân mạch hóa. Cơ chế chủ yếu đến từ:
- Tác dụng điều hòa miễn dịch toàn thân của MSC truyền tĩnh mạch
- Tác dụng cận tiết của hiPSC-CM cấy nội cơ tim, hơn là tái tạo cơ tim trực tiếp.
Không ghi nhận u hay rối loạn nhịp liên quan ghép tế bào, xác nhận tính an toàn của liệu pháp. Việc tăng biểu hiện HLA-G1 trên MSC giúp tăng thêm hiệu quả sửa chữa cơ tim. Nghiên cứu củng cố tiềm năng ứng dụng lâm sàng của phối hợp truyền MSC toàn thân và ghép tế bào cơ tim để phục hồi tim sau nhồi máu.
Hạn chế của nghiên cứu
Nghiên cứu tồn tại một số hạn chế. Thứ nhất, MSC được truyền tĩnh mạch 7 ngày trước khi gây nhồi máu cơ tim dựa trên dữ liệu trước đó cho thấy Treg đạt đỉnh sau 7 ngày, nhưng cỡ mẫu nhỏ và khó mô phỏng hoàn toàn tình trạng lâm sàng; vì vậy thời điểm truyền MSC tối ưu trong thực hành cần được nghiên cứu thêm. Thứ hai, dù tiêm MSC nhiều lần có thể hiệu quả hơn tiêm đơn liều, vẫn chưa rõ việc truyền hUCB-MSC định kỳ mỗi 7 ngày có tăng thêm tác dụng điều hòa miễn dịch hay không; tuy nhiên tăng biểu hiện HLA-G1 đã cho thấy cải thiện rõ hiệu quả này. Thứ ba, do chuột không có phân tử tương đồng HLA-G ở người, nghiên cứu chưa thể làm rõ con đường tín hiệu nền tảng, dù vẫn xác nhận được tác động điều hòa NK và Treg. Thứ tư, khó đánh giá liệu rằng truyền MSC tăng HLA-G1 có làm tăng HLA-G toàn thân trong mô hình chuột, nhưng kết quả cho thấy giảm đáng kể cytokine tiền viêm ở tế bào CD4+ lách. Thứ năm, rối loạn nhịp muộn hoặc thoáng qua chưa thể loại trừ vì chỉ theo dõi ở ngày 7 và 28; tính an toàn cần được kiểm chứng thêm tiền lâm sàng. Cuối cùng, hiệu quả điều trị mới được đánh giá đến ngày 28, nên độ bền vững lâu dài vẫn cần tiếp tục khảo sát.
Kết luận
Tóm lại, nghiên cứu này cho thấy hUCB-MSC tăng biểu hiện gen HLA-G1 có hiệu quả điều hòa miễn dịch vượt trội. Truyền tĩnh mạch hUCB-MSC tăng HLA-G1 giúp tăng khả năng bám ghép của hiPSC-CM được ghép nội cơ tim và cải thiện chức năng tim thông qua việc tăng Treg hệ thống, giảm tế bào NK hệ thống và điều hòa sự phóng thích cytokine miễn dịch. Các nghiên cứu trong tương lai cần được triển khai nhằm xác định đường đưa hUCB-MSC tối ưu trước khi chuyển giao sang ứng dụng lâm sàng.
Tài liệu tham khảo
Zhu W, Kong J, Li HX, Jiang TB, Sun SJ, Zou C (2026). Immunomodulatory effect of mesenchymal stromal cell overexpressing HLA-G1 in cell-based therapy for myocardial infarction. Stem Cell Res Ther. Jan 8;17(1):73.
Nguồn: Stem Cell Res Ther
Link: https://link.springer.com/article/10.1186/s13287-026-04897-7