Int J Med Sci, 01/01/2026
Giới thiệu
Đột quỵ vẫn là một trong những nguyên nhân hàng đầu gây tử vong và tàn tật lâu dài trên toàn cầu, với gánh nặng bệnh tật gia tăng trong thập kỷ qua. Mặc dù đã có những tiến bộ trong các liệu pháp can thiệp sớm như chất hoạt hóa plasminogen mô (tissue Plasminogen Activator, tPA) và lấy huyết khối cơ học, các lựa chọn điều trị vẫn còn hạn chế, và nhiều bệnh nhân vẫn phải đối mặt với các di chứng thần kinh kéo dài. Các liệu pháp dựa trên tế bào gốc, với tiềm năng thúc đẩy tái tạo mô, sửa chữa neuron bị tổn thương và phục hồi các chức năng đã mất thông qua kích thích tạo thần kinh (neurogenesis) và tạo mạch (angiogenesis), đang nổi lên như một hướng tiếp cận đầy hứa hẹn trong điều trị đột quỵ. Các nghiên cứu gần đây cho thấy tế bào gốc có thể di chuyển đến các vùng não bị tổn thương, biệt hóa thành tế bào thần kinh và hòa nhập vào các mạng lưới thần kinh hiện có, từ đó có thể cải thiện khả năng phục hồi chức năng.
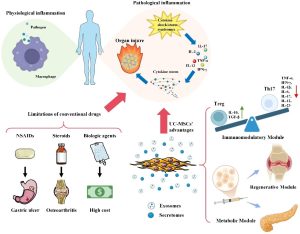
Tế bào gốc trung mô (Mesenchymal Stem Cells, MSCs) là một trong những loại tế bào gốc được sử dụng phổ biến nhất, đã cho thấy tiềm năng trong phục hồi sau đột quỵ trong các nghiên cứu tiền lâm sàng. Trong số các loại MSCs, tế bào gốc trung mô có nguồn gốc từ dây rốn (Umbilical Cord–derived MSCs, UCMSCs) ngày càng được quan tâm do dễ phân lập, tính sinh miễn dịch thấp và khả năng tái tạo mạnh mẽ. UCMSCs có thể di chuyển đến vị trí tổn thương thông qua cơ chế hướng đích bởi chemokine và thúc đẩy sửa chữa mô thông qua tín hiệu cận tiết (paracrine signaling). Các tế bào này phát huy tác dụng điều trị bằng cách điều hòa đáp ứng viêm, tăng cường tạo mạch và thúc đẩy tái tạo thần kinh, từ đó góp phần vào quá trình phục hồi chức năng sau đột quỵ. Hơn nữa, UCMSCs có hồ sơ đánh giá tính an toàn thuận lợi khiến chúng trở thành một ứng viên đầy triển vọng cho ứng dụng lâm sàng.
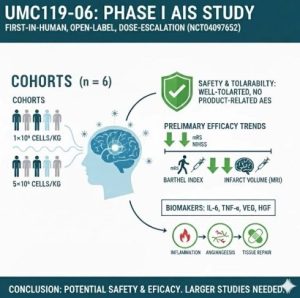
Mặc dù các kết quả tiền lâm sàng rất khả quan, vẫn có ít các thử nghiệm lâm sàng khảo sát việc ứng dụng điều trị của UCMSCs trong đột quỵ thiếu máu não cấp (Acute Ischemic Stroke – AIS). Sự không đồng nhất trong bệnh sinh của đột quỵ, sự khác biệt trong phác đồ điều trị và những thách thức trong việc chuẩn hóa các liệu pháp dựa trên tế bào đã cản trở tiến triển trong lĩnh vực này. Nhằm đáp ứng nhu cầu điều trị chưa được thỏa mãn, chúng tôi đã khởi xướng một nghiên cứu pha I, nhãn mở, tăng liều, lần đầu trên người nhằm đánh giá tính an toàn và khả năng dung nạp của UMC119-06, một sản phẩm UCMSCs, ở bệnh nhân AIS.
Mục tiêu chính là đánh giá tính an toàn, khả năng dung nạp và liều tối đa khả thi (Maximum Feasible Dose – MFD) của UMC119-06. Các mục tiêu phụ bao gồm đánh giá tính an toàn dài hạn và hiệu quả lâm sàng bước đầu sau một lần truyền tĩnh mạch duy nhất UMC119-06. Ngoài ra, nghiên cứu còn khảo sát tác động của UMC119-06 lên các dấu ấn sinh học liên quan đến đột quỵ, qua đó có thể cung cấp thêm hiểu biết về cơ chế tác dụng và lợi ích điều trị tiềm năng của chế phẩm này. Cuối cùng, nghiên cứu nhằm cung cấp dữ liệu nền tảng để định hướng cho các nghiên cứu tiếp theo về các liệu pháp dựa trên UCMSCs trong điều trị AIS.
Phương pháp
Phê duyệt đề cương, đăng ký thử nghiệm và chấp thuận tham gia nghiên cứu
Đề cương thử nghiệm UMC119-06 (mã đăng ký ClinicalTrials.gov: NCT04097652) đã được phê duyệt bởi Cơ quan Quản lý Thực phẩm và Dược phẩm Đài Loan và Hội đồng Đạo đức trong nghiên cứu y sinh của Bệnh viện Shuang Ho – Đại học Y Đài Bắc. Nghiên cứu được thực hiện phù hợp với Tuyên bố Helsinki, và tất cả người tham gia (hoặc người đại diện hợp pháp) đều đã ký đồng thuận tham gia nghiên cứu sau khi được giải thích đầy đủ về mục tiêu, quy trình và các nguy cơ liên quan.
Thiết kế thử nghiệm và giám sát nghiên cứu
Đây là thử nghiệm lâm sàng pha I, nhãn mở, tăng liều, nhằm đánh giá tính an toàn, khả năng dung nạp và liều tối đa khả thi (MFD) của UMC119-06 ở bệnh nhân đột quỵ thiếu máu não cấp (AIS). Nghiên cứu áp dụng thiết kế tăng liều chuẩn 3+3, trong đó mỗi mức liều đều có liều thăm dò ban đầu (sentinel dosing) để đánh giá an toàn trước khi mở rộng tuyển chọn bệnh nhân. Việc tăng lên nhóm liều tiếp theo được cho phép khi 0/3 bệnh nhân hoặc ≤1/6 bệnh nhân xuất hiện độc tính giới hạn liều (DLT); ngược lại, việc tuyển chọn bệnh nhân sẽ dừng nếu có ≥2 bệnh nhân gặp DLT. Sơ đồ thiết kế thử nghiệm được trình bày ở Hình 1.
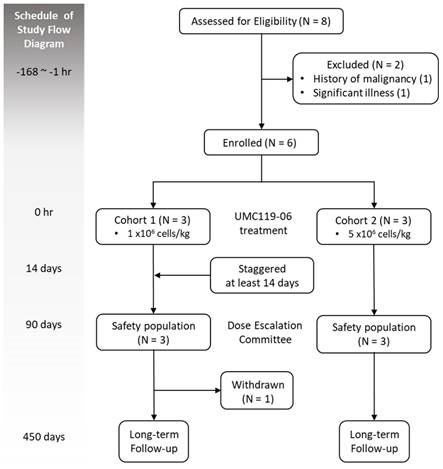
Hình 1. Sơ đồ minh họa thiết kế thử nghiệm và quy trình giám sát nghiên cứu
UMC119-06 là chế phẩm tế bào gốc trung mô có nguồn gốc từ dây rốn người, được sản xuất tại phòng thí nghiệm đạt chuẩn Good Tissue Practice (GTP) dành cho liệu pháp tế bào (Reon Biotech, Đài Loan). Sản phẩm được pha trong dung dịch NaCl 0,9% có bổ sung 2% albumin huyết thanh người đạt chuẩn lâm sàng, với mật độ tế bào từ 3,3×10⁵ đến 2,3×10⁶ tế bào/mL.
Việc lựa chọn liều dùng trên người được xây dựng dựa trên các nghiên cứu tiền lâm sàng trên động vật với ba mức liều khác nhau và không ghi nhận vấn đề an toàn đáng kể. Để chuyển đổi sang liều lâm sàng phù hợp, nhóm nghiên cứu đã áp dụng các nguyên tắc quy đổi liều theo sinh học liên loài (allometric scaling), có xét đến sự khác biệt về khối lượng cơ thể, phân bố tế bào, cũng như khả năng sống và hoạt lực của chế phẩm cuối cùng. Trong nghiên cứu này, bệnh nhân đủ điều kiện được phân vào nhóm liều 1 (1×10⁶ tế bào/kg) hoặc nhóm liều 2 (5×10⁶ tế bào/kg) và được truyền tĩnh mạch một lần duy nhất UMC119-06.
Đối tượng tham gia nghiên cứu
Bệnh nhân đủ điều kiện có độ tuổi từ 20–80, khởi phát đột quỵ trong vòng 48–168 giờ trước khi bắt đầu điều trị, với nguyên nhân do xơ vữa động mạch lớn hoặc thuyên tắc tim. Trước điều trị, bệnh nhân phải có điểm modified Rankin Scale (mRS) 0–1, điểm NIHSS từ 5 đến 20, và không tăng ≥4 điểm NIHSS so với thời điểm nền. Tổn thương nhồi máu vỏ não bán cầu được xác nhận bằng MRI não, với thể tích tổn thương <100 mL trên chuỗi khuếch tán (DWI).
Các tiêu chí loại trừ bao gồm: chuyển dạng xuất huyết trên CT, nhồi máu ổ khuyết hoặc thân não, cơn co giật, hoặc chấn thương sọ não nặng (điểm Glasgow từ 3–8). Ngoài ra, bệnh nhân có tăng huyết áp chưa kiểm soát, rối loạn đông máu chưa được điều chỉnh, tiền sử ung thư, phẫu thuật lớn trong vòng 30 ngày, đang mang thai, nhiễm HIV hoặc bệnh lý nghiêm trọng khác cũng bị loại trừ.
Quy trình thử nghiệm
Nghiên cứu được thực hiện tại Bệnh viện Shuang Ho (Đài Loan). Bệnh nhân đủ điều kiện được phân vào hai nhóm liều và được truyền tĩnh mạch một liều duy nhất UMC119-06 sau khi ghi nhận các thông số nền. Bệnh nhân được theo dõi nội trú 14 ngày để đánh giá độc tính giới hạn liều, và dữ liệu an toàn được Hội đồng Tăng liều (DEC) xem xét trước khi tiếp tục tuyển bệnh hoặc tăng liều. Đánh giá lâm sàng được thực hiện trong 3 tháng sau điều trị, kèm theo dõi an toàn đến 1 năm; nghiên cứu không có phân tích hiệu quả tạm thời.
Đánh giá tiêu chí nghiên cứu
Tiêu chí chính của nghiên cứu là tính an toàn, khả năng dung nạp và liều tối đa khả thi (MFD) của UMC119-06 ở bệnh nhân đột quỵ thiếu máu não cấp. An toàn được theo dõi xuyên suốt thông qua dấu hiệu sinh tồn, xét nghiệm cận lâm sàng, điện tâm đồ, khám lâm sàng và các biến cố bất lợi (AE/TEAE). MFD được xác định dựa trên sự xuất hiện của độc tính giới hạn liều (DLT) trong các TEAE, với dữ liệu được Hội đồng Tăng liều (DEC) xem xét ở từng nhóm liều.
Tiêu chí phụ là mức độ cải thiện chức năng lâm sàng, được đánh giá bằng sự thay đổi của mRS, NIHSS, chỉ số Barthel (BI) và thể tích vùng nhồi máu trên MRI não. Trong đó, mRS và BI phản ánh mức độ phụ thuộc trong sinh hoạt hằng ngày, NIHSS đánh giá mức độ thiếu sót thần kinh do đột quỵ. Thể tích nhồi máu được đo trên MRI bằng phần mềm RAPID, với vùng có ADC < 620 được xác định là mô nhồi máu.
Biến cố bất lợi
Theo quy định 21 CFR 312.32(a), biến cố bất lợi (AE) được định nghĩa là bất kỳ dấu hiệu, triệu chứng hoặc bệnh lý không mong muốn nào xảy ra sau điều trị, do bệnh nhân báo cáo hoặc là sự nặng lên của bệnh lý sẵn có, không nhất thiết phải liên quan đến thuốc/nghiệm pháp nghiên cứu.
Mọi bất thường trên khám lâm sàng hoặc xét nghiệm được điều tra viên đánh giá là có ý nghĩa lâm sàng và xuất hiện sau khi bắt đầu điều trị đều được ghi nhận là AE.
Phân tích thống kê
Nghiên cứu chủ yếu sử dụng phân tích mô tả cho dữ liệu an toàn, có thể thực hiện phân tích suy luận thăm dò với mức ý nghĩa p = 0,05, sử dụng phần mềm SAS và GraphPad Prism để xử lý và trình bày dữ liệu.
Kết quả
Đặc điểm bệnh nhân
Trong số 8 bệnh nhân được sàng lọc, có 6 bệnh nhân được tuyển vào nghiên cứu (mỗi nhóm liều 3 người), trong đó 1 bệnh nhân ở nhóm liều thấp rút lui sớm, và 5 bệnh nhân hoàn tất nghiên cứu; cả 6 bệnh nhân đều được đưa vào phân tích an toàn. 66,7% là nữ, tuổi trung bình 64,0 ± 9,8, cân nặng trung bình 64,4 ± 8,7 kg. Tất cả bệnh nhân đều có tăng huyết áp, kèm theo đái tháo đường (4/6), rối loạn lipid máu (5/6), rung nhĩ (1/6) và tiền sử đột quỵ (2/6); điểm NIHSS trung vị 9,5 (5–17).
Kết quả an toàn
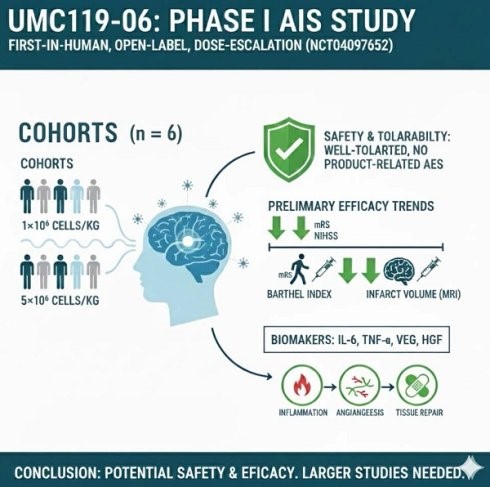
UMC119-06 được đánh giá ở hai mức liều 1×10⁶ và 5×10⁶ tế bào/kg; trong số 6 bệnh nhân, 83,3% có AE/TEAE và 66,7% có SAE, nhưng không ghi nhận độc tính giới hạn liều (DLT). Tất cả TEAE và SAE đều được đánh giá là không hoặc khó liên quan đến thuốc nghiên cứu, chủ yếu liên quan đến nhiễm trùng và biến chứng hô hấp; không có trường hợp tử vong và không phát hiện vấn đề an toàn đáng kể liên quan đến UMC119-06.
Kết quả hiệu quả
Chức năng lâm sàng được đánh giá bằng mRS, NIHSS, chỉ số Barthel (BI) và MRI não cho thấy xu hướng cải thiện rõ rệt sau điều trị. Đến cuối theo dõi (ngày 450), đa số bệnh nhân đạt mRS 0–1, BI đạt 85–100 (gần như độc lập hoàn toàn), và điểm NIHSS giảm >3 điểm từ ngày 30, với mức cải thiện tốt hơn ở nhóm liều cao. MRI não cho thấy giảm đáng kể thể tích nhồi máu, trong đó 5/6 bệnh nhân đạt thể tích 0 mL từ ngày 30 và bệnh nhân còn lại đạt từ ngày 90, duy trì ổn định về sau, gợi ý phục hồi mô não thuận lợi sau điều trị UMC119-06.
Kết quả thăm dò – dấu ấn sinh học
Các dấu ấn sinh học liên quan đến đột quỵ thiếu máu não cấp (AIS), bao gồm Interleukin-1 beta (IL-1β), Interleukin-6 (IL-6), Interferon gamma (IFN-γ), yếu tố hoại tử u alpha (Tumor Necrosis Factor alpha, TNF-α), yếu tố tăng trưởng nội mô mạch máu (Vascular Endothelial Growth Factor, VEGF) và yếu tố tăng trưởng tế bào gan (Hepatocyte Growth Factor, HGF), đã được đánh giá trong suốt quá trình nghiên cứu. Trong số các dấu ấn này, IL-1β và IFN-γ hầu hết không phát hiện được.
Từ ngày 0 đến ngày 30, nồng độ IL-6 tăng lên, với mức tăng trung bình 24,8 pg/mL, trong khi TNF-α chỉ tăng nhẹ 0,8 pg/mL trong cùng khoảng thời gian. Cả VEGF và HGF đều đạt đỉnh vào ngày thứ 7 và sau đó giảm dần theo thời gian. Mức thay đổi trung bình của VEGF từ ngày 0 đến ngày 90 tăng 50,2 pg/mL, trong khi nồng độ HGF giảm 40,9 pg/mL trong cùng giai đoạn.
Thảo luận
Nghiên cứu pha I cho thấy UMC119-06 dung nạp tốt, không ghi nhận độc tính giới hạn liều, và không có biến cố nghiêm trọng nào được xác định là liên quan trực tiếp đến thuốc nghiên cứu. Mặc dù tỷ lệ AE và SAE cao, các biến cố này chủ yếu phù hợp với biến chứng thường gặp ở bệnh nhân sau đột quỵ và không cho thấy xu hướng phụ thuộc liều, qua đó ủng hộ việc tiếp tục phát triển lâm sàng chế phẩm.
Về hiệu quả, nghiên cứu ghi nhận xu hướng cải thiện chức năng thần kinh và khả năng sinh hoạt độc lập, cùng với giảm thể tích nhồi máu trên MRI, gợi ý tiềm năng bảo vệ và phục hồi mô thần kinh của UCMSC. Các kết quả này phù hợp với một số nghiên cứu trước đây về MSC trong đột quỵ, đặc biệt khi điều trị ở giai đoạn sớm, và cho thấy nguồn gốc tế bào (UCMSC so với MSC tự thân) có thể ảnh hưởng đến hiệu quả điều trị.
Các thay đổi dấu ấn sinh học cho thấy UMC119-06 có thể tác động thông qua điều hòa miễn dịch, thúc đẩy tạo mạch và sửa chữa mô, với sự tăng sớm của VEGF và HGF và biến đổi của IL-6, TNF-α, phản ánh vai trò trong quá trình viêm và tái tạo sau thiếu máu não.
Tuy nhiên, nghiên cứu có nhiều hạn chế gồm cỡ mẫu rất nhỏ, thiết kế nhãn mở không có nhóm chứng, và chưa kiểm soát đầy đủ các yếu tố ảnh hưởng đến hồi phục, do đó chưa thể khẳng định chắc chắn hiệu quả điều trị. Các nghiên cứu tiếp theo cần có quy mô lớn hơn, thiết kế đối chứng và theo dõi dài hạn để xác định rõ tính an toàn, liều tối ưu và hiệu quả thực sự của UCMSC trong điều trị AIS, cũng như làm rõ hơn cơ chế tác dụng sinh học thông qua các dấu ấn sinh học.
Kết luận
Nghiên cứu pha I cho thấy UMC119-06 (nguồn gốc từ tế bào gốc trung mô dây rốn người – UCMSCs) an toàn và dung nạp tốt ở bệnh nhân nhồi máu não cấp (AIS), có tín hiệu hiệu quả bước đầu; tuy nhiên cần các thử nghiệm ngẫu nhiên quy mô lớn để xác nhận hiệu quả, tối ưu liều và cách dùng, làm rõ cơ chế qua các dấu ấn sinh học, và tiếp tục theo dõi chặt chẽ biến cố bất lợi nghiêm trọng trước khi áp dụng rộng rãi trên lâm sàng.
Tài liệu tham khảo
Chan, L., Chen, J.H., Hong, C.T., Lin, Y.C., Chang, J.H., Chen, C.C., Hsuan, Y.C.Y., Hu, C.J. (2026). A Phase I, Open-Label, Dose-Escalation Study to Evaluate the Safety and Tolerability of Intravenous UMC119-06 in Patients with Acute Ischemic Stroke. International Journal of Medical Sciences, 23(2), 576-584.
Nguồn: International Journal of Medical Sciences