Open life sciences, 20/03/2026
Giới thiệu
Xơ phổi là nhóm rối loạn phổi với đặc trưng là tích tụ quá mức mô xơ, gây sẹo vĩnh viễn, giảm độ đàn hồi và suy giảm chức năng hô hấp. Xơ phổi vô căn (Idiopathic Pulmonary Fibrosis – IPF) là dạng phổ biến và nghiêm trọng nhất, chủ yếu ở người lớn tuổi, có liên quan đến yếu tố di truyền, môi trường, nghề nghiệp và một số thuốc như bleomycin, amiodarone, methotrexate. Hoạt hóa và xâm nhập bạch cầu thúc đẩy lắng đọng collagen qua cytokine và chemokine proinflammatory, cho thấy vai trò quan trọng của miễn dịch trong tiến triển bệnh.
Tế bào gốc trung mô (Mesenchymal Stem Cells – MSCs) từ tủy xương (BM-MSCs) và dây rốn (UC-MSCs) có khả năng biệt hóa và điều hòa miễn dịch, cải thiện hình thái phổi và chức năng hô hấp trong mô hình IPF nhờ tác dụng chống xơ và chống viêm. Tuy nhiên, các nghiên cứu so sánh hiệu quả và cơ chế giữa hai loại MSCs còn hạn chế. Khảo sát tiềm năng của BM-MSCs và UC-MSCs là cần thiết để tối ưu hóa chiến lược điều trị IPF.
Vật liệu và phương pháp
Mô hình động vật và điều kiện nuôi dưỡng
Nghiên cứu sử dụng chuột đực BALB/c 7–8 tuần và nuôi trong môi trường sạch mầm bệnh với nhiệt độ 23–25 °C, độ ẩm ổn định, chế độ ăn cân bằng và nước tự do. Thí nghiệm, bao gồm gây xơ phổi bằng bleomycin, tuân thủ hướng dẫn đạo đức và được Ủy ban Đạo đức Thú y của trường phê duyệt (Số 2429).
Thiết kế thí nghiệm trên động vật
Chuẩn bị và đặc tính của tế bào gốc trung mô (MSCs)
Trong nghiên cứu này, mục tiêu chính là đánh giá hiệu quả điều trị của UC-MSCs và BM-MSCs trên chuột bị xơ phổi do bleomycin. UC-MSCs được phân lập từ dây rốn của các ca sinh từ phụ nữ khỏe mạnh 30 tuổi cùng sự đồng thuận. Dây rốn được xử lý trong vòng 24 giờ sau sinh: rửa DPBS, khử trùng bằng ethanol 75 %, loại bỏ mạch máu, và cắt nhỏ Wharton’s jelly (0,5–1 mm³). Mẫu được nuôi trong α-MEM với 5 % UltraGRO™ và kháng sinh, 37 °C, 5 % CO2, thay môi trường 3–4 ngày/lần. Khi tế bào đạt mật độ, được tách bằng TrypLE™ Express và mở rộng nuôi cấy. Tế bào P3 được bảo quản trong CryoStor CS10 ở −190 °C. BM-MSCs được lấy từ tủy xương của người hiến khỏe mạnh (24–42 tuổi) qua hút xương chậu. Tế bào đơn nhân được tách bằng Ficoll-Paque và nuôi trong α-MEM với 10 % FBS và kháng sinh; tế bào không bám được loại bỏ sau 48–72 h, các MSCs bám dính được mở rộng và dùng ở P3.
Tiêu chí chọn người hiến gồm không mắc bệnh viêm mạn tính, tự miễn, nhiễm trùng hoặc ác tính; loại trừ người có bệnh toàn thân, dùng thuốc dài hạn hoặc kết quả xét nghiệm bất thường.
Thiết kế thí nghiệm trên động vật và phương pháp điều trị
Tổng cộng 24 chuột đực BALB/c được chia ngẫu nhiên thành 4 nhóm:
- Nhóm kiểm soát (CON): Tiêm saline qua đường khí quản vào ngày 0 và 14.
- Nhóm bleomycin (BLE): Tiêm bleomycin 5 mg/kg vào ngày 0 và saline vào ngày 14.
- Nhóm UC-MSC: Tiêm bleomycin vào ngày 0, sau đó tiêm 1 × 10⁶ UC-MSCs qua đường khí quản vào ngày 14.
- Nhóm BM-MSC: Tiêm bleomycin vào ngày 0, sau đó tiêm 1 × 10⁶ BM-MSCs qua đường khí quản vào ngày 14.
Các chuột được giám sát hàng ngày và euthanasia sớm nếu giảm >15 % trọng lượng, ăn kém hoặc biểu hiện stress. Vào ngày 42, tất cả chuột được euthanasia để thu mô phổi và dịch rửa phế quản (BALF) phục vụ phân tích xơ hóa, viêm và xâm nhập bạch cầu; dịch BALF được ly tâm, phần dịch trên bảo quản −80 °C để đo cytokine, phần bã tế bào dùng phân loại bạch cầu bằng flow cytometry.
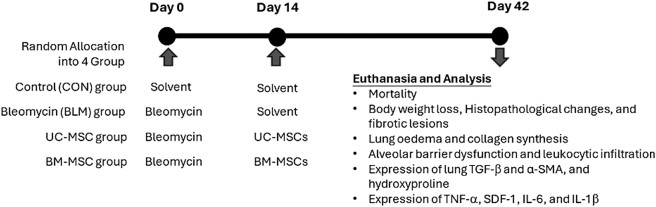
Hình 1. Sơ đồ quy trình thí nghiệm trên mô hình xơ phổi do bleomycin, điều trị bằng UC-MSCs hoặc BM-MSCs
Giám sát tử vong ở động vật
Sau khi tiêm bleomycin để gây xơ phổi, giám sát tử vong của chuột trong 42 ngày. Các chỉ số sinh lý, bao gồm nhịp tim, hô hấp, phản xạ mắt và cử động cơ thể tổng thể, được đánh giá để xác định tình trạng tử vong.
Phân tích trọng lượng mô phổi và chỉ số phổi
Sau khi euthanasia, mô phổi của chuột được cắt ra và cân trọng lượng ướt. Mô sau đó được sấy ở 80 °C trong 48 giờ để xác định trọng lượng khô. Mức độ phù phổi được đánh giá định lượng bằng tỷ lệ ướt/khô (trọng lượng ướt chia cho trọng lượng khô). Chỉ số phổi, phản ánh phì đại phổi so với trọng lượng cơ thể, được tính bằng trọng lượng ướt phổi (mg) chia cho trọng lượng cơ thể (g).
Chuẩn bị mô phổi
Vào ngày 42, mô phổi được cắt và ngâm trong formalin 10 %, bao paraffin và cắt lát vi mô. Lát cắt được nhuộm H&E hoặc Masson’s trichrome để đánh giá cấu trúc tế bào và mô xơ. Xơ hóa được định lượng bằng điểm Ashcroft (0–8) và tỷ lệ diện tích mô xơ so với tổng diện tích trường quan sát (%), cho phép so sánh mức độ xơ giữa các nhóm.
Phân tích miễn dịch mô học (Immunohistochemistry)
Các lát cắt phổi được tẩy paraffin và hồi dịch để chuẩn bị nhuộm. Kháng nguyên được khôi phục bằng dung dịch EDTA, đồng thời sử dụng hydrogen peroxide để giảm nhuộm không đặc hiệu. Sau khi chặn, lát cắt được ủ với kháng thể chính nhận biết TNFα và α-SMA (biomarker của tế bào cơ trơn), sau đó ủ với kháng thể thứ cấp gắn peroxidase. Diaminobenzidine được dùng làm chất phát màu, tạo kết tủa nâu tại vị trí biểu hiện kháng nguyên. Lát cắt sau đó được phân tích bằng kính hiển vi tự động Lion Heart FX.
Phương pháp ELISA (Enzyme-Linked Immunosorbent Assay)
Phương pháp ELISA được thực hiện để định lượng collagen, hydroxyproline, SDF-1 và TGF-β trong mẫu mô phổi. Mẫu được đông lạnh, đồng nhất và ly tâm 5.000×g trong 10 phút ở 4 °C để tách dịch trên, sau đó sử dụng trong các bộ kit ELISA tương ứng. Đồng thời, dịch rửa phế quản (BALF) được phân tích bằng ELISA để đo TNF-α, IL-1β và IL-6.
Xâm nhập bạch cầu trong dịch rửa phế quản (BALF)
Xâm nhập bạch cầu trong dịch rửa phế quản (BALF) được đánh giá bằng flow cytometry. Sau khi ly tâm, bã tế bào được huyền dịch trong PBS chứa 1 % albumin bò. Để phân loại miễn dịch, tế bào được ủ với kháng thể gắn fluorochrome nhận biết các dấu hiệu bề mặt: CD45 (bạch cầu toàn phần), CD11b (tế bào myeloid), Ly6G (tế bào neutrophil) và CD3 (tế bào T). Bạch cầu được xác định là CD45+, granulocyte là CD45+CD11b+, neutrophil là CD45+Ly6G+, lymphocyte là CD45+CD3+. Phân tích flow cytometry bao gồm mẫu chứng không nhuộm và chứng đồng loại để xác định tín hiệu nền và thiết lập gating. Tế bào nhuộm được hoàn nguyên trong PBS và phân tích bằng máy Accuri C6 với phần mềm đi kèm.
Phân tích thống kê
Phân tích thống kê được thực hiện bằng SPSS. Dữ liệu biểu thị dưới dạng trung bình ± SD. Phân phối chuẩn kiểm định bằng Shapiro-Wilk; ANOVA + Bonferroni dùng cho dữ liệu chuẩn, Kruskal-Wallis + Dunn dùng cho dữ liệu không chuẩn. Ý nghĩa thống kê: so với CON # P < 0,05; so với BLE *P < 0,05; so với UC-MSC $ P < 0,05.
Kết quả
Giảm tỷ lệ tử vong do xơ phổi gây ra bởi bleomycin nhờ UC-MSCs và BM-MSCs
Để đánh giá hiệu quả của UC-MSCs và BM-MSCs trong giảm tử vong do xơ phổi gây bởi bleomycin, chuột được điều trị MSCs vào ngày 14 sau khi tiêm bleomycin. Tỷ lệ tử vong được ghi nhận hàng ngày trong 42 ngày. Nhóm BLE có tỷ lệ tử vong cao hơn đáng kể so với nhóm CON, trong khi UC-MSCs giảm tử vong hiệu quả hơn BM-MSCs.
Ảnh hưởng của UC-MSCs và BM-MSCs lên cân nặng, thay đổi mô bệnh học và tổn thương xơ hóa
Kết quả cho thấy bleomycin gây giảm cân rõ rệt (P < 0,05). Điều trị bằng UC-MSCs, nhưng không phải BM-MSCs, làm giảm đáng kể tình trạng giảm cân do bleomycin. Thay đổi mô bệnh học đánh giá bằng nhuộm H&E cho thấy tổn thương cấu trúc phổi, dày thành phế nang và xâm nhập bạch cầu rõ hơn ở nhóm BLE so với nhóm CON. Cả UC-MSCs và BM-MSCs đều cải thiện đáng kể các thay đổi mô học và điểm Ashcroft (P < 0,05). Vùng tổn thương xơ hóa, đánh giá bằng nhuộm Masson’s trichrome, nhiều hơn ở nhóm BLE; cả hai MSCs đều giảm xơ hóa đáng kể (P < 0,05), nhưng UC-MSCs cho hiệu quả vượt trội trong giảm xơ và phục hồi cấu trúc phổi.
Ảnh hưởng của UC-MSCs và BM-MSCs lên phù phổi và tổng hợp collagen
Chỉ số phổi và tỷ lệ ướt/khô là các chỉ số chính để đánh giá phù phổi trong mô hình IPF. Bleomycin gây phù phổi rõ rệt, được cải thiện đáng kể sau điều trị bằng UC-MSCs hoặc BM-MSCs (P < 0,05). Biểu hiện collagen tăng đáng kể sau bleomycin và giảm rõ rệt sau điều trị UC-MSCs, trong khi BM-MSCs không mang lại hiệu quả tương tự (P < 0,05).
Giảm rối loạn chức năng hàng rào phế nang và xâm nhập bạch cầu sau can thiệp bằng UC-MSCs và BM-MSCs
Rối loạn chức năng hàng rào phế nang được đánh giá dựa trên nồng độ protein trong BALF. Bleomycin gây rối loạn hàng rào phế nang rõ rệt (P < 0,05), được cải thiện đáng kể sau điều trị bằng UC-MSCs nhưng không bằng BM-MSCs. Rối loạn này cho phép bạch cầu, bao gồm granulocyte, neutrophil và lymphocyte, xâm nhập mô phổi, thúc đẩy phản ứng viêm. Xâm nhập bạch cầu, granulocyte, neutrophil và lymphocyte tăng đáng kể sau bleomycin (P < 0,05), nhưng điều trị bằng UC-MSCs hoặc BM-MSCs đều cải thiện đáng kể tình trạng xâm nhập bạch cầu vào các tổn thương xơ hóa (P < 0,05).
Giảm biểu hiện TGF-β, α-SMA và hydroxyproline phổi nhờ UC-MSCs
Trong nghiên cứu tiến triển xơ phổi, nhóm BLE có biểu hiện tăng của các dấu ấn chống xơ TGF-β và α-SMA, phù hợp với xơ hóa tiến triển. Phân tích miễn dịch mô học cho thấy UC-MSCs làm giảm rõ rệt TGF-β và α-SMA, trong khi BM-MSCs chỉ giảm hạn chế. Phân tích ELISA cho thấy cả hai MSCs giảm đáng kể TGF-β trong mô phổi (P < 0,05), nhưng chỉ UC-MSCs giảm đáng kể hydroxyproline (P < 0,05), chỉ dấu tích lũy collagen. Kết quả nhấn mạnh hiệu quả chống xơ vượt trội của UC-MSCs, ức chế TGF-β và giảm tích lũy collagen cùng hoạt động myofibroblast, trong khi BM-MSCs cải thiện hạn chế.
Ảnh hưởng của UC-MSCs và BM-MSCs lên biểu hiện TNF-α, SDF-1, IL-6 và IL-1β
Phân tích ELISA cho thấy TNF-α, SDF-1, IL-6 và IL-1β trong BALF tăng đáng kể ở nhóm BLE so với CON (P < 0,05). Cả UC-MSCs và BM-MSCs đều giảm TNF-α đáng kể (P < 0,05), trong khi chỉ UC-MSCs mới làm giảm đáng kể SDF-1, IL-6 và IL-1β (P < 0,05).
Thảo luận
- IPF và mô hình nghiên cứu
- IPF là bệnh phổi tiến triển, đặc trưng bởi xơ hóa, khó thở, ho khan, mệt mỏi; chủ yếu ảnh hưởng người 70–75 tuổi, tuổi thọ trung bình 2–5 năm sau chẩn đoán.
- Nguyên nhân chưa rõ, tiến triển không đồng nhất, hạn chế điều trị hiệu quả.
- Mô hình bleomycin ở chuột tái tạo các đặc trưng của IPF: giảm cân, phù phổi, tổn thương xơ hóa, tăng collagen, thay đổi mô học.
- Hiệu quả của UC-MSCs và BM-MSCs
- Tỷ lệ tử vong: Cả UC-MSCs và BM-MSCs giảm tử vong so với nhóm BLE, nhưng UC-MSCs hiệu quả hơn.
- Cân nặng & cấu trúc phổi: UC-MSCs phục hồi cân nặng và cấu trúc phổi tốt hơn BM-MSCs.
- Xơ hóa & mô học: UC-MSCs giảm đáng kể fibrotic lesions, collagen, TGF-β, α-SMA, hydroxyproline; BM-MSCs giảm TGF-β và α-SMA nhưng không giảm hydroxyproline.
- Alveolar barrier & viêm: UC-MSCs cải thiện chức năng hàng rào phế nang, giảm xâm nhập bạch cầu và cytokine proinflammatory (TNF-α, SDF-1, IL-6, IL-1β) mạnh hơn BM-MSCs.
- Cơ chế & lợi thế của UC-MSCs
- Khả năng sinh sản cao, miễn dịch thấp, ổn định gen.
- Điều hòa cytokine, giảm TGF-β, NF-κB, Wnt/β-catenin → giảm xơ hóa và viêm.
- BM-MSCs có tác dụng hạn chế hơn, đặc biệt với hydroxyproline và tái tạo cấu trúc phổi.
- Hạn chế nghiên cứu
- Mô hình bleomycin chưa hoàn toàn tái tạo IPF ở người.
- Chỉ dùng một liều, một lịch trình, chưa đánh giá phân bố lâu dài, tồn tại tế bào, hay các cytokine điều hòa như IL-10.
- Cần nghiên cứu bổ sung để xác nhận hiệu quả lâm sàng của UC-MSCs và BM-MSCs.
Kết luận
Nghiên cứu này xác nhận rằng các đặc điểm bệnh lý của IPF do bleomycin gây ra, bao gồm tử vong, giảm cân và xơ hóa phổi, có thể tái tạo ở chuột. Việc sử dụng UC-MSCs làm giảm đáng kể tử vong, giảm cân, tổn thương mô học, tổn thương xơ hóa, tích tụ collagen và biểu hiện TGF-β, α-SMA, hydroxyproline, đồng thời cải thiện phù phổi, xâm nhập bạch cầu, rối loạn hàng rào phế nang và cytokine tiền viêm. BM-MSCs chỉ mang lại cải thiện một phần, chủ yếu giảm phù phổi, xâm nhập bạch cầu và biểu hiện TNF-α, nhưng kém hiệu quả hơn UC-MSCs. Kết quả cho thấy UC-MSCs có hiệu quả điều trị vượt trội so với BM-MSCs trong IPF do bleomycin.
Tài liệu tham khảo
Ni, Y. L., Shen, H. T., Lee, C. Y., Lee, T. P., Sieber, M., Tseng, C. C., Tsao, C. T., & Kuan, Y. H. (2026). UC-MSCs exhibit superior antifibrotic and anti-inflammatory effects compared to BM-MSCs in a bleomycin-induced idiopathic pulmonary fibrosis model. Open life sciences, 21(1), 20251293.
Nguồn: Open life sciences









