Health Science Reports, 08/02/2026
Giới thiệu
Các bệnh lý thận ở trẻ em bao gồm nhiều rối loạn khác nhau, như bệnh thận mạn (CKD), tổn thương thận cấp (AKI), viêm cầu thận, hội chứng thận hư và các dị tật bẩm sinh của thận và đường tiết niệu (CAKUT). Những bệnh lý này có thể ảnh hưởng đáng kể đến sự tăng trưởng, phát triển và sức khỏe tổng thể của trẻ, thường dẫn đến các biến chứng lâu dài và làm giảm chất lượng cuộc sống. Các phương pháp điều trị hiện nay chủ yếu tập trung vào kiểm soát triệu chứng và làm chậm tiến triển bệnh, nhưng thường không giải quyết được nguyên nhân căn bản cũng như không thúc đẩy quá trình tái tạo mô.
Trong những năm gần đây, liệu pháp tế bào gốc đã thu hút nhiều sự quan tâm như một hướng tiếp cận tiềm năng mang tính đột phá trong điều trị các bệnh thận. Trong số các loại tế bào gốc, tế bào gốc trung mô (MSCs) nổi lên như những ứng viên đầy triển vọng cho các ứng dụng điều trị trong thận học nhi khoa. MSCs là các tế bào gốc đa năng, có thể được phân lập từ tủy xương, mô mỡ, dây rốn và tủy răng. Những tế bào này có nhiều đặc tính thuận lợi cho y học tái tạo, bao gồm khả năng tự làm mới, biệt hóa thành nhiều dòng tế bào khác nhau và điều hòa đáp ứng miễn dịch.
Bài tổng quan này tập trung trình bày các nghiên cứu hiện tại về tiềm năng ứng dụng MSCs trong điều trị các bệnh thận ở trẻ em. Cụ thể, chúng tôi tổng hợp các nghiên cứu tiền lâm sàng và lâm sàng liên quan đến liệu pháp MSC cho nhiều bệnh lý thận khác nhau, phân tích các cơ chế tác động và thảo luận những lợi ích cũng như thách thức của hướng điều trị mới này.
Tế bào gốc trung mô: Đặc điểm và nguồn gốc
- Tế bào gốc trung mô (Mesenchymal Stem Cells – MSCs) là các tế bào gốc đa năng có khả năng tự làm mới và biệt hóa thành xương, sụn và mỡ. Theo tiêu chuẩn của ISCT, MSCs phải bám dính khi nuôi cấy, biểu hiện các dấu ấn sinh học CD73, CD90, CD105 và không biểu hiện các marker huyết học như CD45, CD34, HLA-DR.
- MSCs có tiềm năng điều trị bệnh thận nhờ khả năng điều hòa miễn dịch, chống viêm, ức chế tế bào T, ảnh hưởng đến tế bào B và tế bào tua. Ngoài ra, chúng còn tiết các yếu tố tăng trưởng và cytokine giúp tăng sự sống sót tế bào, tăng sinh và tân sinh mạch. MSCs cũng có tính sinh miễn dịch thấp, nên ít gây thải ghép.
- Nhiều nguồn MSCs khác nhau có thể được sử dụng cho mục đích điều trị các bệnh thận ở trẻ em, mỗi nguồn đều có những ưu điểm và hạn chế riêng. MSCs có nguồn gốc từ tủy xương (BM-MSCs) đã được nghiên cứu rộng rãi và cho thấy kết quả khả quan trong điều trị bệnh thận. Tuy nhiên, thủ thuật hút tủy xương mang tính xâm lấn, có thể hạn chế việc áp dụng ở bệnh nhân nhi khoa. MSCs có nguồn gốc từ mô mỡ (AD-MSCs) là nguồn tế bào dễ tiếp cận hơn, có thể thu nhận thông qua các thủ thuật ít xâm lấn và trong một số nghiên cứu cho thấy hiệu quả điều trị tương đương BM-MSCs. MSCs có nguồn gốc từ dây rốn (UC-MSCs) có nhiều ưu điểm như thu nhận không xâm lấn, khả năng tăng sinh cao và có thể sở hữu đặc tính điều hòa miễn dịch vượt trội so với MSCs có nguồn gốc từ mô trưởng thành.
- Khi lựa chọn nguồn MSCs cho điều trị bệnh thận ở trẻ em cần cân nhắc khả năng thu nhận, tiềm năng tăng sinh, đặc tính điều hòa miễn dịch và khả năng tái tạo mô; hiệu quả điều trị có thể khác nhau tùy nguồn tế bào và mô hình bệnh.
Cơ chế tác động của tế bào gốc trung mô trong các bệnh lý thận
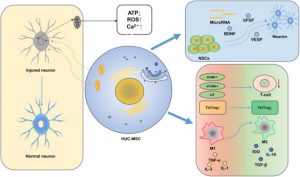
- Điều hòa miễn dịch: MSCs ức chế hoạt hóa và tăng sinh tế bào T, thúc đẩy Treg, ức chế tế bào B và tế bào tua, đồng thời chuyển đại thực bào từ kiểu viêm M1 → M2 chống viêm.
- Hỗ trợ tái tạo mô: tiết các yếu tố tăng trưởng giúp tế bào thận sống sót, tăng sinh, hình thành mạch máu mới và có thể chuyển ty thể khỏe mạnh sang tế bào bị tổn thương.
- Chống xơ hóa thận: ức chế quá trình EMT (Epithelial-to-Mesenchymal Transition), giảm hình thành nguyên bào sợi và thúc đẩy phân giải chất nền ngoại bào.
- Tác dụng cận tiết: tiết nhiều yếu tố tăng trưởng và cytokine chống viêm (HGF, IGF-1, EGF, IL-10, TGF-β) và giải phóng túi ngoại bào/exosome, giúp truyền tín hiệu và thúc đẩy phục hồi mô.
Các cách thức sử dụng liệu pháp MSC trong các rối loạn thận ở trẻ em
- Đường tĩnh mạch (IV): phương pháp phổ biến, ít xâm lấn, phù hợp cho trẻ em; MSCs di chuyển đến mô tổn thương qua trục SDF-1/CXCR4. Tuy nhiên, hiệu quả đến thận thấp do hiệu ứng “qua phổi lần đầu” (pulmonary first-pass effect), chỉ khoảng 2–5% tế bào tới thận.
- Đường toàn thân: tận dụng tác dụng cận tiết của MSCs như exosome để điều hòa miễn dịch và làm chậm tiến triển bệnh (CKD, hội chứng thận hư). Có thể dùng lặp lại nhưng vẫn gặp hạn chế tương tự đường IV như khả năng định vị thận thấp và nguy cơ đáp ứng miễn dịch khi dùng MSC dị ghép.
- Đưa tại chỗ: tiêm động mạch thận hoặc trong nhu mô/dưới bao thận, giúp tăng tỷ lệ MSC đến thận (10–20%). Có thể hỗ trợ sửa chữa mô thận và giảm protein niệu, nhưng xâm lấn hơn, cần can thiệp kỹ thuật và có nguy cơ chảy máu, nhiễm trùng.
- Tiêm trực tiếp vào thận: đưa MSCs trực tiếp vào nhu mô thận, đạt nồng độ tế bào cao tại vị trí tổn thương và hiệu quả trong tổn thương cầu thận. Tuy nhiên rất xâm lấn, rủi ro thủ thuật cao và ít tác động đến viêm toàn thân.
Lựa chọn cách thức sử dụng MSC cần cân bằng giữa hiệu quả điều trị, mức độ xâm lấn và độ an toàn ở trẻ em; nghiên cứu tương lai nên cải thiện khả năng homing của MSCs và phát triển phương pháp đưa tối ưu cho bệnh thận nhi khoa.
Các nghiên cứu tiền lâm sàng về liệu pháp tế bào gốc trung mô trong các bệnh lý thận ở trẻ em
Nghiên cứu tiền lâm sàng (trên mô hình động vật) cho thấy MSCs có khả năng giảm tổn thương thận, giảm viêm và thúc đẩy tái tạo mô trong các bệnh thận ở trẻ em.
- Bệnh thận mạn (CKD): MSCs giúp làm chậm tiến triển bệnh, giảm xơ hóa thận, giảm lắng đọng chất nền ngoại bào (ECM) và điều hòa đáp ứng miễn dịch.
- Tổn thương thận cấp (AKI):
+ Trong mô hình thiếu máu – tái tưới máu (IRI) ở chuột, BM-MSCs (1–2 × 106 tế bào, tiêm tĩnh mạch) giúp giảm creatinine huyết thanh 30–50% và giảm các cytokine viêm (TNF-α, IL-6).
+ UC-MSCs trong mô hình AKI do cisplatin giúp giảm chết theo chu trình (apoptosis), giảm stress oxy hóa và cải thiện GFR.
- CKD trong mô hình cắt 5/6 thận: AD-MSCs (2 × 106 tế bào, nội phúc mạc) giúp giảm xơ hóa kẽ, giảm protein niệu (~40%) và giảm lượng nitơ urê trong máu (Blood Urea Nitrogen – BUN).
- Bệnh cầu thận: UC-MSCs (1 × 106 tế bào, tiêm tĩnh mạch) trong mô hình anti-Thy1 glomerulonephritis giúp giảm protein niệu, giảm viêm cầu thận và bảo vệ tế bào chân giả (podocyte).
- Dị tật bẩm sinh thận (UUO): nghiên cứu trên động vật trưởng thành cho thấy MSCs có thể giảm xơ hóa và bảo tồn quá trình tạo nephron, nhưng chưa có nhiều nghiên cứu trên mô hình sơ sinh.
Nhiều mô hình động vật (IRI, cắt thận, UUO) với các loại MSCs khác nhau (BM-MSCs, UC-MSCs, AD-MSCs) và các chỉ số đánh giá (creatinine, GFR, protein niệu, mô học) đã tạo cơ sở tiền lâm sàng vững chắc cho việc phát triển liệu pháp MSC trong bệnh thận nhi khoa.
Các nghiên cứu lâm sàng về liệu pháp tế bào gốc trung mô trong các bệnh lý thận ở trẻ em
Các nghiên cứu lâm sàng ban đầu cho thấy liệu pháp MSCs có tiềm năng an toàn và hiệu quả trong điều trị bệnh thận ở trẻ em, bao gồm AKI, CKD, bệnh cầu thận và CAKUT.
- Tổn thương thận cấp (Acute Kidney Injury – AKI):
+ Thử nghiệm pha I ở trẻ 2–12 tuổi (n=15) dùng BM-MSCs dị ghép tiêm tĩnh mạch (1×10⁶ tế bào/kg).
+ Creatinine giảm ~25% sau 7 ngày, nhu cầu lọc máu giảm từ 40% xuống 20%, không ghi nhận biến cố bất lợi nghiêm trọng.
- Bệnh thận mạn tính (Chronic Kidney Disease – CKD):
+ Nghiên cứu pha I ở trẻ 5–15 tuổi (n=12) dùng UC-MSCs (2×10⁶ tế bào/kg).
+ eGFR ổn định trong 6 tháng, ACR giảm ~30%, tác dụng phụ nhẹ (sốt nhẹ ~10%).
- Hội chứng thận hư kháng steroid (SRNS):
+ Trẻ 3–10 tuổi (n=10) dùng AD-MSCs tự thân (1×10⁶ tế bào/kg).
+ Protein niệu giảm ~40% sau 3 tháng, albumin huyết thanh tăng, phù cải thiện ở 60% bệnh nhân.
- CAKUT (Congenital Anomalies of the Kidney and Urinary Tract – Dị tật bẩm sinh của hệ tiết niệu):
+ Các nghiên cứu liên quan đến cơ chế Wnt/β-catenin cho thấy MSCs có tiềm năng cải thiện cấu trúc thận.
+ Ghi nhận tăng độ dày vỏ thận ~20% và giảm mức độ ứ nước thận trong 6 tháng.
Dữ liệu lâm sàng ban đầu cho thấy MSCs có thể cải thiện chức năng thận và ổn định bệnh, với độ an toàn tương đối cao, nhưng cần nghiên cứu lớn hơn và theo dõi dài hạn để xác nhận hiệu quả.
Ngoài các bằng chứng lâm sàng ban đầu đã được ghi nhận, những tiến bộ trong giai đoạn 2023–2024 tiếp tục củng cố và mở rộng hiểu biết về tiềm năng của liệu pháp MSC trong điều trị các bệnh lý thận ở trẻ em. MSCs được xem là có triển vọng điều trị lớn nhờ đặc tính tái tạo mô và điều hòa miễn dịch, đặc biệt trong bối cảnh tỷ lệ tử vong do tổn thương thận cấp (AKI) trên toàn cầu vẫn ở mức cao (20–50%). Các tế bào này có khả năng làm giảm viêm thận thông qua việc ức chế sự trưởng thành của tế bào tua (dendritic cells), từ đó hạn chế phản ứng viêm liên quan đến tiến triển của bệnh. Gần đây, một hướng tiếp cận mới là sử dụng các túi ngoại bào có nguồn gốc từ MSCs (MSC-derived extracellular vesicles – MSC-EVs) với kích thước khoảng 30–100 nm, có tác dụng chống viêm, chống lão hóa và hỗ trợ quá trình lành mô. Nhờ những đặc tính này, MSC-EVs được xem là một liệu pháp “không tế bào” đầy hứa hẹn, với ưu điểm về tính ổn định và độ an toàn cao hơn so với liệu pháp tế bào trực tiếp, đặc biệt phù hợp cho điều trị bệnh thận ở trẻ em.
Liệu pháp tế bào gốc trung mô trong bệnh thận ở người lớn và so sánh với ứng dụng ở trẻ em
- Ở người lớn, liệu pháp MSCs đã được nghiên cứu rộng rãi trong nhiều bệnh thận như AKI, CKD, bệnh cầu thận, bệnh thận sau ghép và bệnh thận do đái tháo đường. MSCs giúp giảm viêm, thúc đẩy sửa chữa ống thận, giảm xơ hóa và cải thiện chức năng thận, chủ yếu thông qua cơ chế cận tiết.
- Thử nghiệm NEPHSTROM (2023) cho thấy MSCs có thể làm chậm sự suy giảm eGFR trong 18 tháng, cho thấy tiềm năng điều trị bệnh thận và mở ra cơ sở tham khảo cho nghiên cứu ở trẻ em.
- Bằng chứng năm 2023 xác nhận MSCs có tác dụng chống chết theo chu trình (apoptosis), chống oxy hóa, chống viêm và chống xơ hóa, một phần nhờ túi ngoại bào (exosomes/EVs). MSCs và EVs cũng có tiềm năng trong AKI do nhiễm virus.
- Tiến bộ riêng cho nhi khoa (2024):
+ EVs từ tế bào thận tự thân (RACev) có thể giảm xơ hóa, viêm và thiếu oxy sau AKI, đồng thời tăng tân tạo mạch.
+ Các thử nghiệm REACT sử dụng phương pháp quy đổi liều theo tương quan kích thước sinh học (allometric scaling) dựa trên khối lượng thận ước tính từ hình ảnh học 3D (3×10⁶ tế bào/g) để cá thể hóa liều điều trị cho trẻ em.
Khác biệt chính giữa ứng dụng MSC ở người lớn và trẻ em
- Nguyên nhân bệnh:
- Người lớn: chủ yếu do đái tháo đường, tăng huyết áp, thiếu máu cục bộ.
- Trẻ em: thường do dị tật bẩm sinh (CAKUT) hoặc bệnh di truyền.
- Mục tiêu điều trị:
- Người lớn: làm chậm hoặc đảo ngược tổn thương thận.
- Trẻ em: hỗ trợ phát triển thận và ngăn tiến triển bệnh sớm.
- Đặc điểm sinh lý và phương pháp điều trị:
- Trẻ em có thận nhỏ, đang phát triển, nhạy cảm hơn với thủ thuật xâm lấn.
- Người lớn có thể dùng tiêm động mạch thận, trong khi trẻ em thường ưu tiên đường tĩnh mạch.
- Tiêu chí đánh giá hiệu quả:
- Người lớn: trì hoãn ESRD hoặc cải thiện GFR.
- Trẻ em: ngoài chức năng thận còn chú trọng tăng trưởng và phát triển lâu dài.
- An toàn và đạo đức:
- Nghiên cứu ở người lớn đã có dữ liệu an toàn rộng hơn.
- Ở trẻ em, nghiên cứu vẫn giai đoạn sớm, cần thận trọng hơn với liệu pháp thử nghiệm và thủ thuật xâm lấn.
Kinh nghiệm từ nghiên cứu ở người lớn cung cấp nền tảng quan trọng cho ứng dụng MSC trong nhi khoa, nhưng cần điều chỉnh về liều lượng, phương pháp đưa tế bào và mục tiêu điều trị để phù hợp với đặc điểm sinh lý và bệnh học của trẻ em.
Kết quả chưa thống nhất và những hạn chế của các thử nghiệm lâm sàng hiện nay
Bằng chứng hiện tại về MSC trong bệnh thận nhi khoa vẫn mang tính sơ bộ. Cần các thử nghiệm lâm sàng lớn hơn, chuẩn hóa phương pháp và theo dõi dài hạn để xác định rõ hiệu quả và độ an toàn của liệu pháp này.
Thách thức và định hướng nghiên cứu trong tương lai
Việc giải quyết các thách thức về nguồn tế bào, phương pháp đưa tế bào, cơ chế tác động, biomarker và tiêu chuẩn nghiên cứu sẽ giúp phát triển liệu pháp MSC cá thể hóa, an toàn và hiệu quả hơn cho trẻ em mắc bệnh thận.
Kết luận
Liệu pháp tế bào gốc trung mô (MSCs) là hướng điều trị đầy tiềm năng cho bệnh thận nhi khoa nhờ các cơ chế như điều hòa miễn dịch, tái tạo mô, chống xơ hóa và tín hiệu cận tiết. Các nghiên cứu tiền lâm sàng và thử nghiệm lâm sàng giai đoạn đầu cho thấy MSCs có thể hỗ trợ điều trị nhiều bệnh thận ở trẻ em như AKI, CKD, bệnh cầu thận và dị tật bẩm sinh hệ tiết niệu (CAKUT).
Tuy nhiên, trước khi áp dụng rộng rãi trong lâm sàng, vẫn còn nhiều thách thức cần giải quyết. Hiệu quả điều trị phụ thuộc vào nguồn MSCs (tủy xương, dây rốn, mô mỡ) và phương pháp đưa tế bào, trong đó tiêm tĩnh mạch thuận tiện nhưng khả năng hướng đích đến thận còn hạn chế. Ngoài ra, việc ứng dụng ở trẻ em cần cân nhắc các yếu tố đặc thù như nguyên nhân bệnh, sự phát triển của cơ quan, mục tiêu điều trị và yêu cầu an toàn cao hơn so với người lớn.
Các hạn chế hiện tại gồm sự không đồng nhất về phương pháp nghiên cứu, cỡ mẫu nhỏ, quy trình khác nhau và thiếu dữ liệu an toàn dài hạn. Do đó, các nghiên cứu trong tương lai cần tập trung vào xác định dấu ấn sinh học đáp ứng điều trị, chuẩn hóa quy trình, phát triển mô hình nghiên cứu đặc hiệu cho trẻ em, tối ưu hóa phương pháp đưa MSCs và xây dựng khung pháp lý phù hợp.
Sự hợp tác giữa bác sĩ thận học, nhà nghiên cứu tế bào gốc và cơ quan quản lý sẽ đóng vai trò quan trọng trong việc chuyển các kết quả nghiên cứu đầy hứa hẹn thành liệu pháp lâm sàng an toàn và hiệu quả, góp phần cải thiện tiên lượng cho trẻ em mắc bệnh thận.
Tài liệu tham khảo
Bahroudi, M., & Moghtaderi, M. (2026). Therapeutic Potential of Mesenchymal Stem Cells in Pediatric Kidney Disorders: A Comprehensive Review. Health science reports, 9(2), e71769.
Nguồn: Health Science Reports
Link: https://onlinelibrary.wiley.com/doi/full/10.1002/hsr2.71769