Journal of Neurorestoratology, 12/02/2026
Giới thiệu
Bại não (Cerebral Palsy – CP) là nhóm rối loạn không tiến triển của hệ thần kinh trung ương, do tổn thương não ở giai đoạn bào thai hoặc sơ sinh, đặc trưng bởi rối loạn vận động và tư thế. Nhiều yếu tố nguy cơ đã được xác định như bệnh não chu sinh, nhiễm trùng trong tử cung, sinh non, dị tật bẩm sinh và phản ứng viêm bất thường của thai nhi. CP không chỉ ảnh hưởng vận động mà còn gây rối loạn ngôn ngữ, nhận thức và tâm lý, tạo gánh nặng lớn về kinh tế và xã hội.
Hiện nay, điều trị chủ yếu gồm phục hồi chức năng, thuốc giảm co cứng và can thiệp phẫu thuật. Tuy nhiên, các phương pháp này chỉ cải thiện triệu chứng, chưa thể phục hồi tổn thương thần kinh nền tảng, nên hiệu quả lâu dài còn hạn chế. Do đó, nhu cầu về các liệu pháp mới có khả năng tái tạo và phục hồi chức năng thần kinh là rất cấp thiết. Trong bối cảnh này, liệu pháp tế bào nổi lên như một hướng tiếp cận đầy tiềm năng trong điều trị các bệnh lý thần kinh, bao gồm bại não.
Liệu pháp ghép tế bào như một hướng tiếp cận của y học tái tạo
Liệu pháp ghép tế bào là một hướng tiếp cận mới nổi trong y học tái tạo, cho thấy tiềm năng lớn trong điều trị nhiều bệnh lý. Tế bào gốc có khả năng tăng sinh, tự làm mới và biệt hóa, với các loại chính được sử dụng gồm: HSCs, ESCs, iPSCs, NSCs và MSCs. Trong đó, tế bào gốc trung mô (Mesenchymal Stromal Cell – MSCs) có khả năng tự làm mới và biệt hóa đa dòng, đã được ứng dụng trong nhiều thử nghiệm lâm sàng. Tuy nhiên, MSCs từ tủy xương hoặc mô mỡ vẫn tồn tại hạn chế như giảm tiềm năng theo tuổi hoặc thu nhận xâm lấn. Ngược lại, tế bào gốc trung mô từ mô dây rốn (Umbilical Cord Mesenchymal Stromal Cell – UC-MSCs) có nhiều ưu điểm nổi bật: nguồn dồi dào, thu nhận không xâm lấn, ít vấn đề đạo đức, tính sinh miễn dịch thấp và an toàn cao, phù hợp cho ứng dụng lâm sàng. Gần đây, UC-MSCs cho thấy hiệu quả đáng kể trong tái tạo và phục hồi thần kinh, thông qua cơ chế tiết yếu tố dinh dưỡng thần kinh, điều hòa miễn dịch và ức chế viêm, mở ra hướng điều trị đầy hứa hẹn cho bại não.
Phương pháp nghiên cứu
Nghiên cứu này sử dụng phương pháp tổng quan tài liệu. Tổng cộng có 32 bài báo được lựa chọn để tổng hợp mô tả về thiết kế nghiên cứu, đặc điểm mẫu, phương pháp can thiệp và các kết quả chính.
Nghiên cứu tiền lâm sàng về tế bào gốc trung mô dây rốn người (human Umbilical Cord Mesenchymal Stromal Cell –hUC-MSCs)
Cơ chế tác động của hUC-MSCs trong phục hồi thần kinh
Thiếu máu–thiếu oxy gây tổn thương não trong bại não bằng cách làm chết oligodendrocyte, mất myelin và hoạt hóa tế bào thần kinh đệm, dẫn đến stress oxy hóa và phản ứng viêm với các cytokine như IL-1, IL-6, TNF-α và IFN-γ. Hệ quả là viêm thần kinh kéo dài, tổn thương hàng rào máu–não, ức chế tái tạo sợi trục và gây tổn thương thứ phát.
Do đó, điều trị cần hướng đến tái tạo myelin, điều hòa viêm và phục hồi mạng lưới thần kinh, thông qua các cơ chế như tái sinh, bảo vệ và tăng tính dẻo thần kinh—đây cũng là cơ sở cho ứng dụng hUC-MSCs.
(Ⅰ) Điều hòa miễn dịch và tái cấu trúc vi môi trường
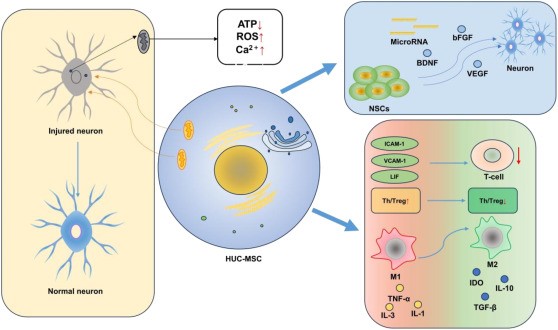
Hình 1. Trong hệ thần kinh trung ương, hUC-MSCs thúc đẩy phục hồi thần kinh thông qua ba cơ chế chính: điều hòa miễn dịch (đỏ–xanh), tín hiệu cận tiết (màu xanh) và chuyển giao bào quan (màu vàng).
hUC-MSCs điều hòa miễn dịch bằng cách ức chế đáp ứng tế bào T, giảm trình diện kháng nguyên và khôi phục cân bằng Th17/Treg. Tại vị trí tổn thương, chúng thúc đẩy chuyển cực M1 → M2, làm giảm cytokine tiền viêm (TNF-α, IL-1β) và tăng yếu tố kháng viêm (IL-10), từ đó giảm viêm thần kinh và hỗ trợ tái tạo mô.
Ngoài ra, hUC-MSCs tiết LIF, TGF-β, IL-10 và IDO, giúp ức chế stress oxy hóa và hoạt hóa tế bào thần kinh đệm, tạo vi môi trường miễn dịch–chuyển hóa thuận lợi cho phục hồi thần kinh theo cơ chế “miễn dịch trước – sửa chữa sau”.
(Ⅱ) Hỗ trợ dinh dưỡng thần kinh và tái tạo thần kinh
hUC-MSCs phát huy tác dụng thông qua cơ chế cận tiết, tiết ra các yếu tố dinh dưỡng thần kinh như BDNF, VEGF và bFGF, giúp tăng sống sót tế bào thần kinh, hỗ trợ phục hồi và thúc đẩy sinh thần kinh mới. Đồng thời, hUC-MSCs hoạt hóa tế bào gốc thần kinh nội sinh (NSCs) và định hướng biệt hóa thành neuron chức năng.
Ngoài ra, hUC-MSCs còn kích thích biểu hiện các microRNA (miR-124, miR-145), góp phần tăng sinh và biệt hóa tế bào tiền thân thần kinh, qua đó thúc đẩy quá trình tái tạo hệ thần kinh.
(Ⅲ) Tăng sinh, tái tạo tế bào và khôi phục chức năng ty thể
Ngoài cơ chế cận tiết, hUC-MSCs còn tham gia trực tiếp vào phục hồi thần kinh thông qua:
- Biệt hóa thần kinh: Trong vi môi trường tổn thương, hUC-MSCs có thể tăng sinh và biệt hóa thành tế bào giống neuron, góp phần thay thế tế bào bị tổn thương và phục hồi chức năng thần kinh.
- Chuyển giao ty thể (Mitochondrial Transfer – MT): Rối loạn chức năng ty thể (giảm OXPHOS, ATP, tăng stress oxy hóa và rối loạn cân bằng Ca²⁺) làm trầm trọng thêm tổn thương thần kinh. hUC-MSCs đóng vai trò nguồn cho ty thể, thiết lập trao đổi bào quan với các tế bào khác, giúp phục hồi sản xuất ATP (~45%) và tăng khả năng tăng sinh của tế bào nhận.
Cơ chế này nhấn mạnh vai trò của ty thể như “yếu tố chức năng” quan trọng trong sửa chữa tế bào và mở ra hướng liệu pháp thay thế bào quan trong điều trị bại não.
Nghiên cứu trên động vật trong điều trị bại não
Các nghiên cứu trên động vật là bước quan trọng nhằm đánh giá hiệu quả, độ an toàn và cơ chế tác động của hUC-MSCs trước khi chuyển sang lâm sàng. Chuột cống và chuột nhắt là mô hình phổ biến, có thể tái hiện rối loạn vận động, nhận thức và tổn thương não tương tự bại não.
Kết quả cho thấy, với liều 5 × 10³ – 5 × 10⁶ tế bào, hUC-MSCs giúp cải thiện vận động và nhận thức, đồng thời giảm thể tích tổn thương não trên MRI và mô học. Ở mức độ tế bào, liệu pháp này giảm hoạt hóa vi bào đệm và tế bào hình sao, ức chế stress oxy hóa (PKA/PKC), giảm tự thực và apoptosis (Beclin-2, caspase-3), và giảm cytokine viêm (TNF-α, IL-1β). Hiệu quả điều trị phụ thuộc vào liều, tần suất, thời điểm và đường dùng: liều cao và tiêm lặp lại cho kết quả tốt hơn; ghép sớm (24 giờ sau tổn thương) hiệu quả hơn ghép muộn; và đường tĩnh mạch cho khả năng di cư vào não cao hơn so với đường khác.
Hạn chế trong việc chuyển giao từ mô hình động vật sang thực hành lâm sàng
Dù hUC-MSCs cho thấy hiệu quả trên mô hình động vật, việc chuyển sang lâm sàng còn hạn chế do khác biệt sinh lý và phát triển não giữa chuột và người, cũng như cấu trúc não phức tạp hơn ở người. Các mô hình hiện tại chưa tái hiện đầy đủ đặc điểm bại não (co cứng, loạn trương lực, nhận thức…), và đánh giá hành vi còn hạn chế. Ngoài ra, khó chuẩn hóa liều tế bào do khác biệt kích thước cơ thể giữa loài.
→ Cần mô hình động vật bậc cao hơn và tối ưu liều, thời điểm, đường dùng để cải thiện khả năng ứng dụng lâm sàng.
Nghiên cứu lâm sàng về hUC-MSCs
Mặc dù dữ liệu lâm sàng về hUC-MSCs trong điều trị bại não còn hạn chế so với tiền lâm sàng, các nghiên cứu gần đây cho thấy tiềm năng đáng kể của liệu pháp tế bào. Các nghiên cứu này cung cấp bằng chứng ban đầu về hiệu quả và độ an toàn của hUC-MSCs, đồng thời tập trung đánh giá các yếu tố quan trọng như liều tế bào, đường dùng, thời điểm điều trị (tuổi bệnh nhân) và hạn chế nghiên cứu.
Liều lượng tế bào
Liều tế bào là yếu tố quan trọng quyết định hiệu quả điều trị. Các nghiên cứu hiện nay cho thấy khoảng liều 1 × 10⁶ – 1 × 10⁷ tế bào/kg được xem là an toàn và hiệu quả. Một nghiên cứu hồi cứu trên 152 bệnh nhân bại não cho thấy liều 1 × 10⁶/kg dung nạp tốt, không ghi nhận biến cố nghiêm trọng và giúp cải thiện chức năng vận động và sức cơ.
Tuy nhiên, liều tối ưu còn phụ thuộc vào đường dùng: đường tĩnh mạch (IV) thường ưu tiên liều thấp hoặc nồng độ thấp để giảm phản ứng truyền, trong khi đường tủy sống (IT) có thể sử dụng liều hoặc nồng độ cao hơn với hiệu quả tiềm năng tốt hơn.
Đường đưa tế bào hUC-MSCs trong điều trị
Các đường đưa hUC-MSCs phổ biến gồm IV, IT, IA, IN và ICV, tuy nhiên chưa có đường tối ưu được xác định.
- ICV: đưa trực tiếp vào não → chính xác, nhanh; nhưng xâm lấn cao, nguy cơ tổn thương và nhiễm trùng, không phù hợp lâm sàng (đặc biệt ở trẻ).
- IA: ít xâm lấn hơn ICV, tận dụng “hiệu ứng đi qua lần đầu vào não, tăng phân bố tế bào; nhưng có nguy cơ tắc mạch, thiếu máu cục bộ, biến chứng tim phổi.
- IV: phổ biến nhất (~80%), an toàn và dễ thực hiện; nhưng tế bào dễ bị giữ lại ở gan, phổi, lách → giảm lượng đến não.
- IT: đưa vào dịch não tủy → tiếp cận trực tiếp hệ thần kinh trung ương; tuy nhiên cần kỹ thuật cao, vô khuẩn nghiêm ngặt, có thể cần gây mê và có nguy cơ biến chứng.
- IN: không xâm lấn, vượt qua hàng rào máu–não; nhưng bị hạn chế bởi phân hủy enzyme, pH niêm mạc và biến thiên cá thể, làm giảm hiệu quả hấp thu.
→ Mỗi đường có ưu/nhược điểm riêng, cần tối ưu hóa tùy mục tiêu điều trị và tình trạng bệnh nhân.
Thời điểm ghép tế bào (tuổi bệnh nhân)
Thời điểm ghép là yếu tố quan trọng ảnh hưởng đến hiệu quả điều trị. Các nghiên cứu hiện nay chủ yếu thực hiện trên bệnh nhi (sơ sinh đến ~16 tuổi), trong đó tuổi càng nhỏ thì đáp ứng càng tốt.
Giai đoạn trước tuổi đi học được xem là “cửa sổ vàng” do hệ thần kinh đang phát triển mạnh, giúp tăng khả năng sửa chữa và tái tổ chức thần kinh. Một nghiên cứu hồi cứu gần đây cũng cho thấy bệnh nhân nhỏ tuổi có đáp ứng điều trị tốt hơn, nhấn mạnh vai trò của can thiệp sớm.
Tính an toàn
hUC-MSCs được đánh giá là tương đối an toàn trong các nghiên cứu lâm sàng, chưa ghi nhận biến cố bất lợi nghiêm trọng. Các tác dụng phụ thường gặp gồm sốt thoáng qua, đau đầu, nôn và đau lưng, đa số tự hồi phục hoặc cải thiện trong vòng 72 giờ với điều trị triệu chứng. Các thử nghiệm lâm sàng ngẫu nhiên đối chứng cũng xác nhận tính an toàn này, với các tác dụng phụ ở mức độ nhẹ và không xuất hiện biến cố mới trong theo dõi dài hạn (12–24 tháng).
Hiệu quả điều trị
hUC-MSCs cho thấy cải thiện rõ rệt chức năng vận động thô ở bệnh nhân bại não. Hiệu quả được đánh giá qua nhiều thang đo và công cụ như GMFM, FMFM, ADL, chất lượng cuộc sống, MRI/DTI, EEG và phân tích mạng não. Các nghiên cứu lâm sàng ghi nhận tăng đáng kể điểm GMFM, FMFM và sức cơ sau điều trị. Hiệu quả có xu hướng tăng theo số đợt điều trị, với bệnh nhân nhận nhiều liệu trình đạt cải thiện tốt hơn.
Ngoài ra, hUC-MSCs giúp giảm trương lực cơ (co cứng), đặc biệt khi kết hợp phục hồi chức năng, từ đó nâng cao khả năng vận động tổng thể.
Phân tích các yếu tố ảnh hưởng đến hiệu quả điều trị
Mối liên quan giữa đặc điểm bệnh nhân và kết quả điều trị
- Ảnh hưởng của cỡ mẫu và tuổi đến chức năng vận động
Kết quả FMFM phụ thuộc vào cỡ mẫu và độ tuổi:
- Mẫu lớn + bệnh nhân nhỏ tuổi → cải thiện rõ hơn (do tính dẻo thần kinh cao).
- Mẫu nhỏ + bệnh nhân lớn tuổi → khó thấy khác biệt, do giảm đáp ứng và hạn chế thống kê.
→ Cần tăng cỡ mẫu và phân tầng tuổi rõ hơn trong nghiên cứu tương lai.
- Vai trò của cỡ mẫu trong sự khác biệt về cải thiện chức năng nhận thức
Cỡ mẫu nhỏ làm tăng ảnh hưởng của biến thiên cá thể, dẫn đến kết quả không đồng nhất giữa các nghiên cứu. Do đó, các nghiên cứu tương lai cần:
- Tăng cỡ mẫu, thiết kế đa trung tâm, đối chứng mù đôi
- Phân tầng độ tuổi chi tiết để giảm sai số
- Chuẩn hóa liều theo cân nặng (cells/kg) để tăng độ chính xác và khả năng ứng dụng lâm sàng
Hạn chế trong các hệ thống đánh giá hiệu quả hiện nay
- Hạn chế của các công cụ đánh giá
- Thời gian theo dõi chưa đủ
Tổng kết và triển vọng
hUC-MSCs có tiềm năng phục hồi thần kinh đáng kể trong CP thông qua điều hòa miễn dịch, giảm viêm và sửa chữa tế bào thần kinh, với bằng chứng ban đầu cho thấy an toàn và hiệu quả ngắn hạn. Tuy nhiên, vẫn cần các nghiên cứu quy mô lớn, đa trung tâm và theo dõi dài hạn để xác nhận. Hiện tại, các thách thức chính bao gồm: hạn chế nguồn tế bào, khả năng định vị kém, hiệu suất sử dụng thấp và khó theo dõi tế bào in vivo. Hướng phát triển tương lai:
- Sản xuất tế bào quy mô lớn, chuẩn hóa quy trình, xây dựng ngân hàng tế bào.
- Tăng độ chính xác trong phân phối tế bào.
- Cải thiện theo dõi tế bào sau ghép (MRI với chất đánh dấu chuyên biệt)
- Tối ưu hệ thống đánh giá hiệu quả bằng cách kết hợp MRI, EEG và AI để phân tích chức năng não và dự đoán đáp ứng điều trị.
Tài liệu tham khảo
Sai Wang, Yachen Wang, Jing Liu (2026). Research progress on the therapeutic efficacy of human umbilical cord mesenchymal stromal cells for cerebral palsy in children. Journal of Neurorestoratology, Volume 14, Issue 2.
Nguồn: Journal of Neurorestoratology
Link: https://www.sciencedirect.com/science/article/pii/S2324242625000889